2026年2月16日に発表された、Heartseed株式会社2025年12月期決算説明の内容を書き起こしでお伝えします。
2025年12月期決算説明
福田恵一氏:みなさまこんにちは。Heartseed株式会社代表取締役社長の福田恵一です。本日は、ご多忙の中、2025年12月期決算説明会にご参加くださいまして、誠にありがとうございます。
はじめに、先週金曜日に、東京証券取引所とJPX総研が「JPXスタートアップ急成長100指数」の新設について発表されましたが、ありがたいことに構成銘柄に選出いただきました。市場のご期待に応えられるよう、心筋再生医療の実用化に向けて着実な事業進捗を示していきたいと思います。
それでは、2月13日に適時開示した期末の決算短信を基に、本日ご説明します。
免責事項
スライドは免責事項です。
本日の目次

本日のアジェンダです。
決算の概要、今期の業績予想、直近のトピックスをお話した後に、質疑応答の時間を取ります。
2025年12月期決算:P/L
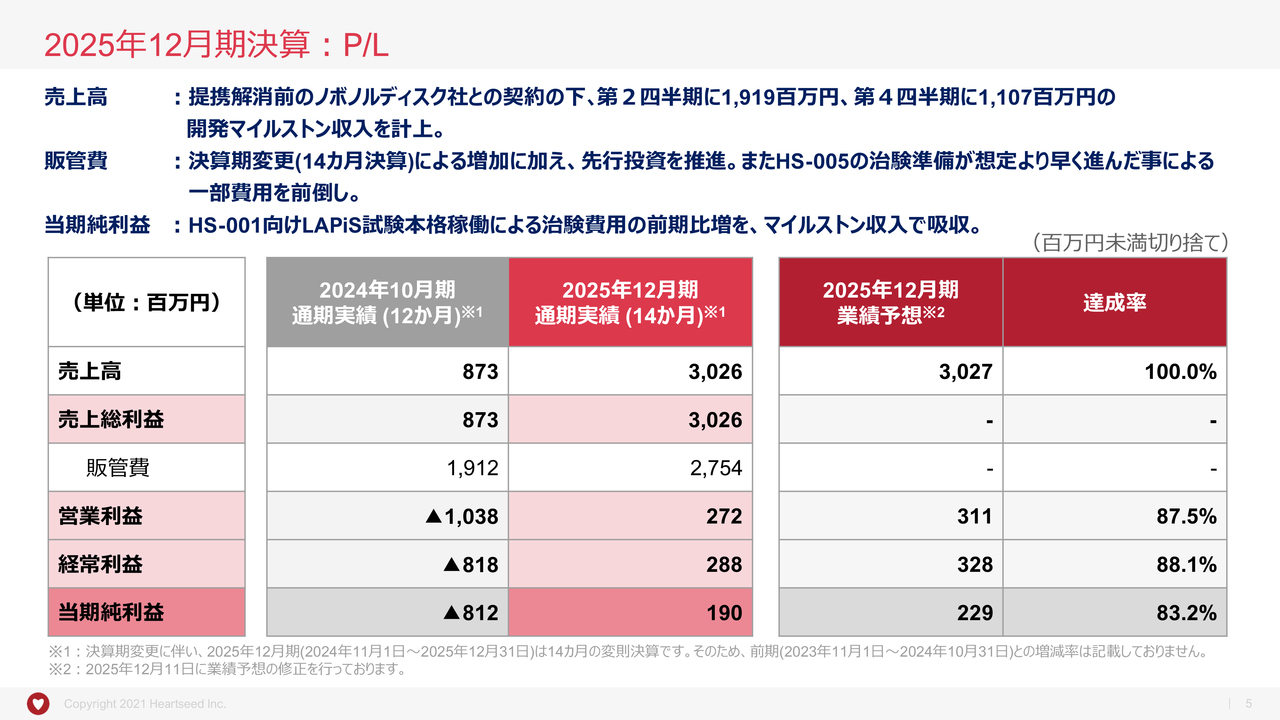
まずは、2025年12月期決算概要です。
はじめにP/Lです。
売上高に関して、提携解消前のノボノルディスク・エーエス社(以下、ノボ社)との提携に基づき、第2四半期に約19億円、第4四半期に約11億円の開発マイルストン収入を計上し、累計で30億2,600万円となりました。昨年12月11日に発表した業績予想どおりとなっています。
売上総利益は、現状、売上原価がありませんので、売上と同様となります。
販管費は、決算期の変更に伴い、2025年12月期が変則的に14ヶ月ありましたので、対前年で大幅増に見えますが、中身は、「HS-001」の治験推進などが順調に進捗したことによる計画どおりの先行投資です。これにくわえて、「HS-005」の国内治験に向けた準備が、年末にかけて想定より早く進んだことにより、一部の費用が前倒しで発生しました。
その結果、営業利益は、2億7,200万円、経常利益は2億8,800万円、純利益は1億9,000万円と、12月11日に発表した業績予想よりもわずかに届きませんでしたが、「HS-001」向け「LAPiS試験」本格稼働による治験費用の前期比増を、マイルストン収入で吸収したかたちとなりました。
2025年12月期決算:B/S
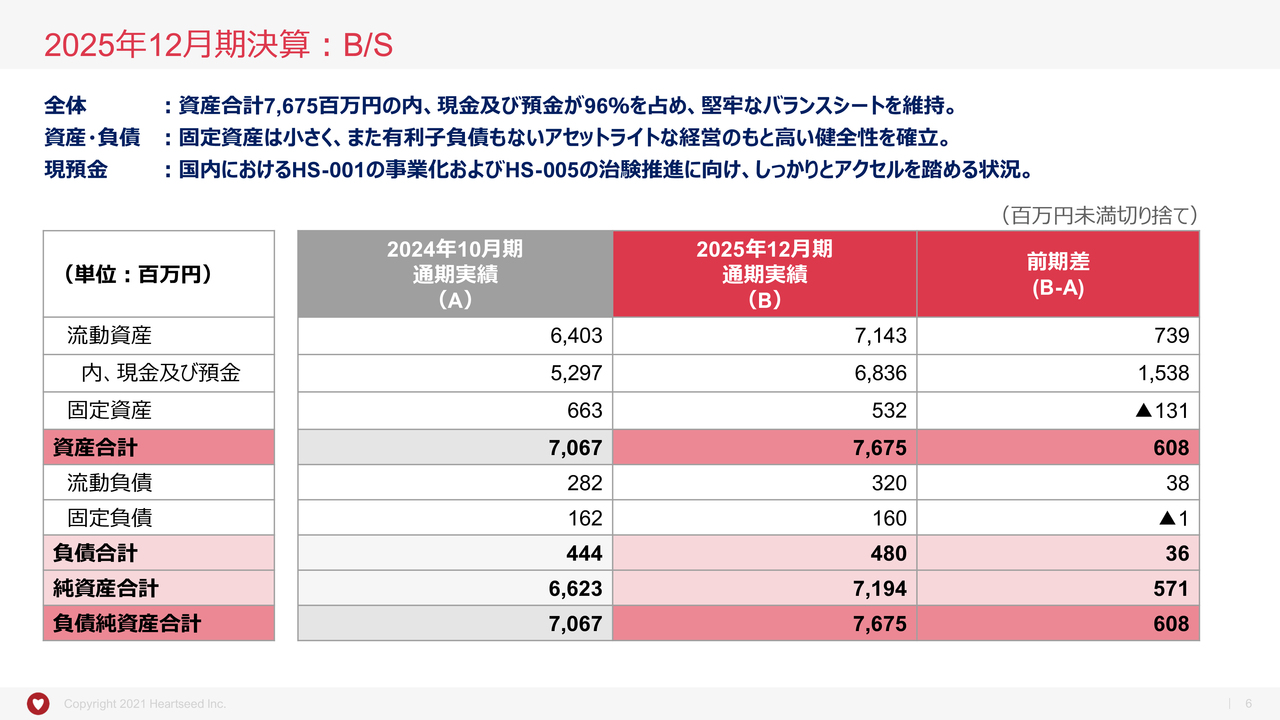
続きまして、B/Sです。
ノボ社からのマイルストン収入が第2四半期と第4四半期にあったことにより前期と比べ現預金が増え、現預金が資産の96パーセントを占めるという、堅牢なバランスシートを維持しています。国内における「HS-001」の事業化および「HS-005」の治験推進に向けて、しっかりとアクセルを踏める財務状況です。
2025年12月期 開発目標に対する進捗

主な事業進捗について説明します。
ノボ社との提携解消後における、技術データやノウハウ等の共同開発資産の内部化・回帰プロセスは、概ね完了しました。
「HS-001」については、「LAPiS試験」における患者投与が完了し、現在経過観察中です。承認申請に向けた準備が計画どおり粛々と進んでいます。そうした中、国内での治験施設医師による学会発表、そして米国AHAなどの国際学会における会社発表を経て、良好な全10例の途中経過を12月に会社発表しました。その内容を受けて、本年度のトピックとはなりますが、世界で最も権威ある国際学術シンポジウムの1つであるKeystone Symposiaに招聘され、世界トップクラスの科学者に対し、当社の技術と臨床データを共有したとともに、未来の方向性を議論しました。
「HS-005」については、日本ライフラインとの協業・提携にくわえ、国内における治験「EMERALD試験」に関して、治験届の審査が無事完了し、複数の治験施設において、患者さまの探索に着手いただいている状況です。今年上期内における1例目の患者投与を目指していきます。
自家iPS細胞から作製する心筋細胞である「HS-040」は、国からの補助金を基に、引き続き技術開発や前臨床試験に向けた準備を進めています。
2026年12月期 業績予想
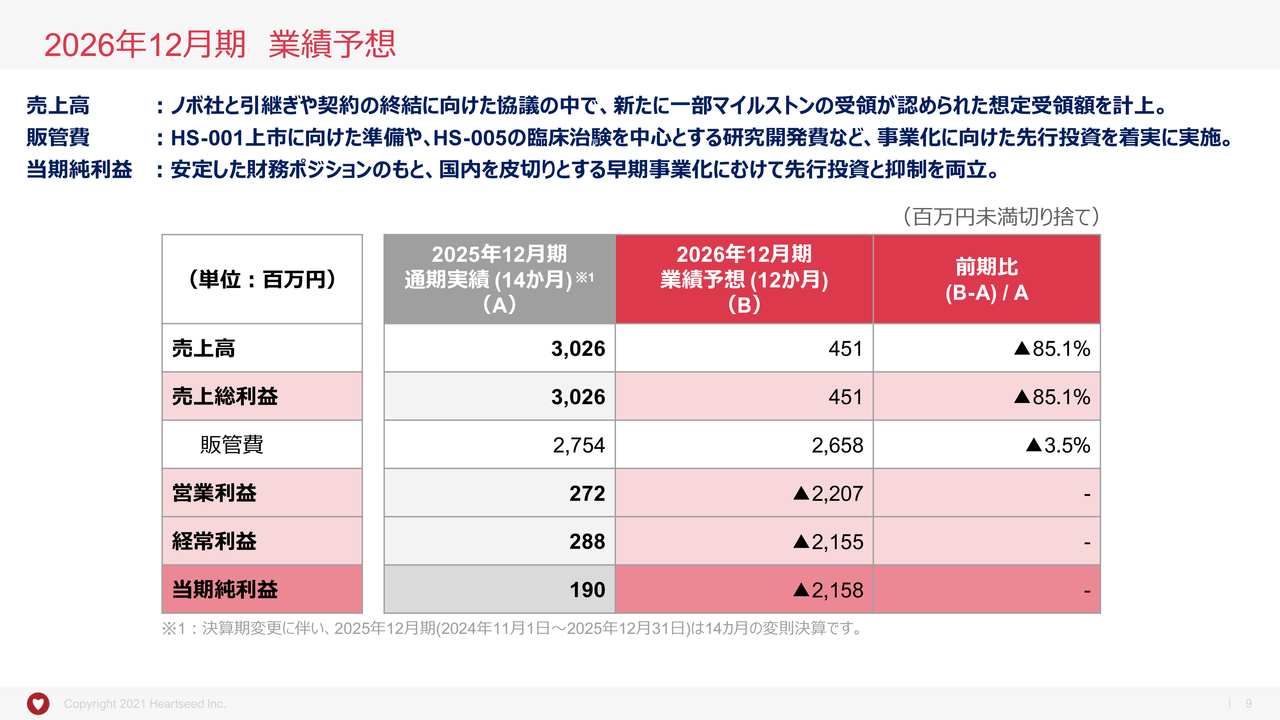
それでは、2026年12月期の業績予想についてご説明します。
売上高に関しては、本年度はマイルストン収入がなくなることで、一旦ゼロとなる想定でいましたが、ノボ社との提携解消後、同社との交渉の結果、新たに一部マイルストンの受領が認められ、売上高4億5,100万円を見込むに至りました。
販管費は、「HS-001」における国内製販体制の整備や「HS-005」における「EMERALD試験」の費用などが増加する一方、「HS-001」の「LAPiS試験」費用が減少することで相殺され、26億5,800万円と、前年並みを想定しています。筋肉質な運営を意識しつつも、国内における事業進捗に向けた先行投資をしっかり行っていく経営方針です。
2026年12月期 パイプラインに関する事業目標

今期の事業目標です。
先ず全体について、詳細はお伝えできませんが、良好な臨床エビデンスが揃いつつある中、それに基づく優位な交渉ポジションを活かし、中長期グローバル戦略の確立を目指します。
「HS-001」に関しては、全10例の1年データの取りまとめや解析を行い、当局との適切な対話の基、2026年内の承認申請を目指していきます。また、来年2027年内の国内上市を目指して、製販体制の整備を進めていきます。
「HS-005」については、上期内での1例目投与を実現し、その後の安全性評価委員会の承認を経て、患者組入れを推進していきます。くわえて、治験施設医師のご理解、ご協力の基、途中経過をアカデミアに対し、また可能であれば株式市場のみなさまへ共有できるよう模索していきます。
「HS-040」は、引き続き国からの補助金を最大限活用しながら、実用化に向けた開発を積み上げていきます。
製品パイプライン
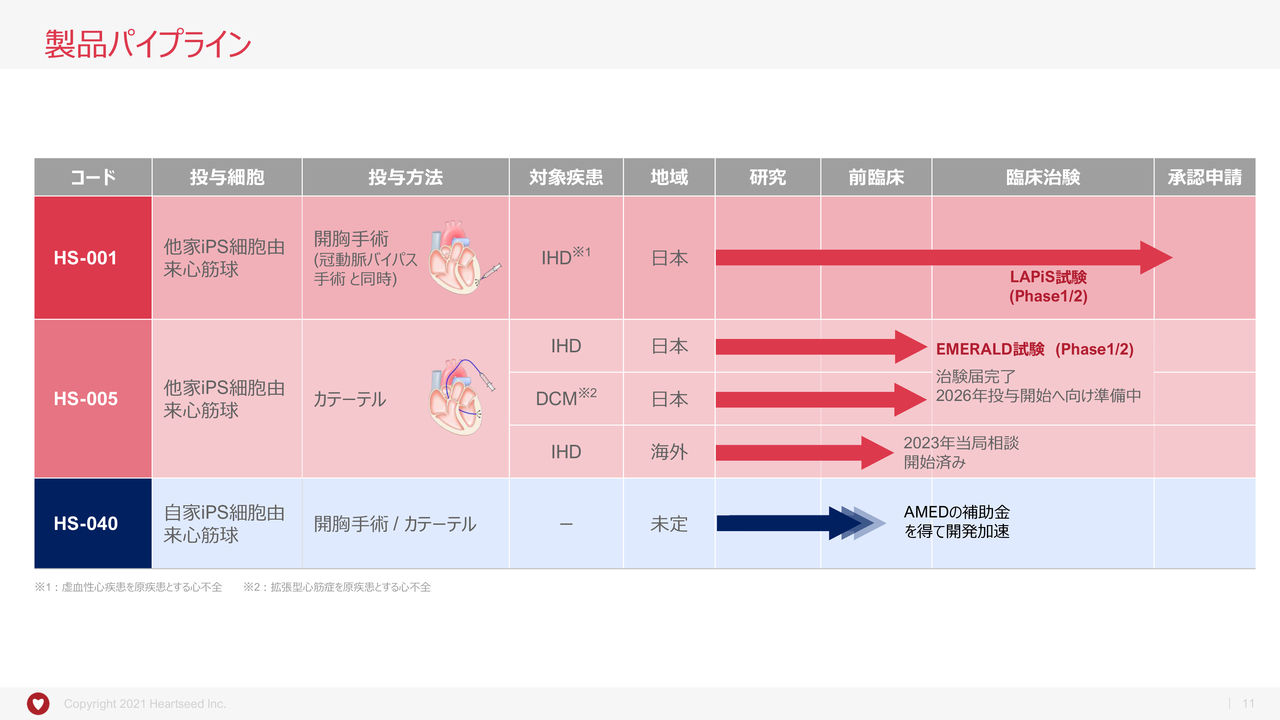
こちらのスライドは、製品パイプラインのおさらいなので説明は割愛します。
メインパイプラインの2か年目標マイルストン(2026年2月13日現在)
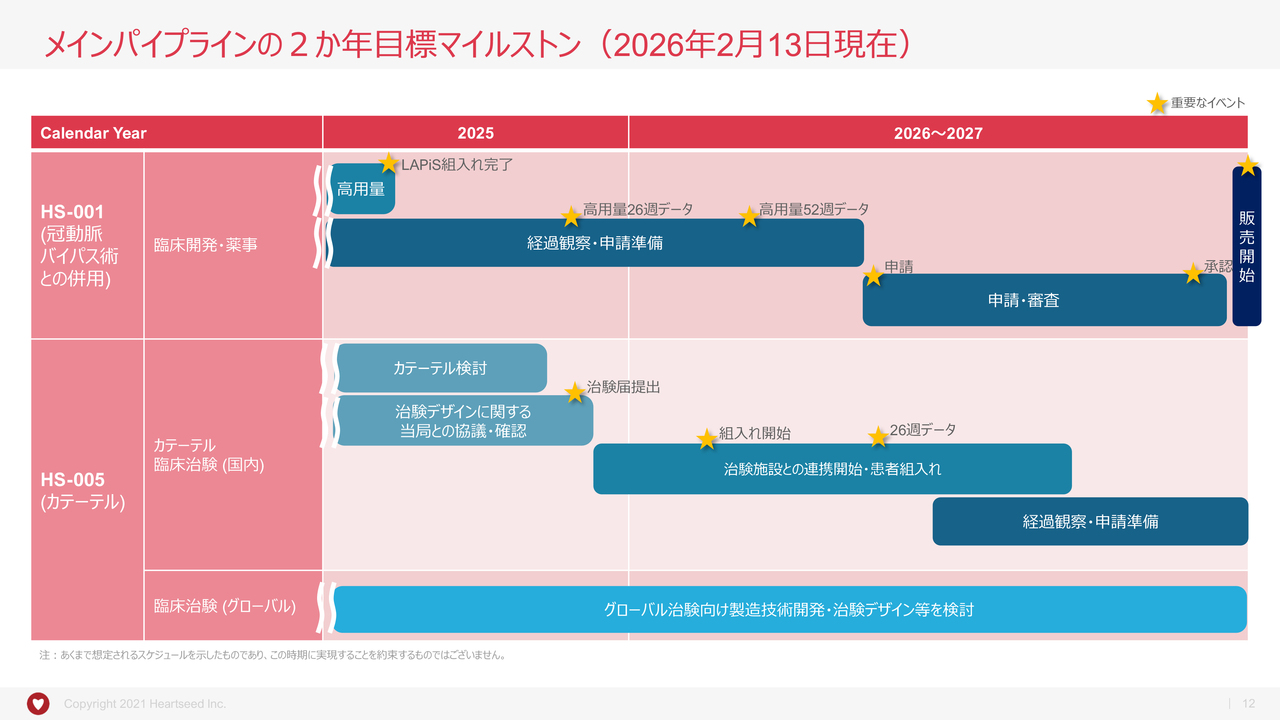
「HS-001」と「HS-005」の具体的なタイムラインです。
「HS-001」に関しては、先月末に全10例の術後1年が経過しました。治験施設さまからデータが寄せられた後、解析と取りまとめが行われ、それらを基にした申請準備へと進むため、多少の時間を要しますが、従前の計画と変わらず、2026年内の承認申請、2027年内の承認および販売開始を目指しています。1日でも早くお待ちいただいている患者さまにお届けできるよう、最善をつくしていきます。
「HS-005」については、前のスライドで触れたように、国内の「EMERALD試験」に関して、現在、複数の治験施設において患者さまの探索に着手いただいた状況です。いずれの治験施設医師も本治験に対し積極的でいらっしゃるように見受けられ、期待したいところではありますが、現時点においては、未だどの程度のスピードで患者組入れが進むのか想定することは時期尚早と考えています。少なくとも上期内に1例目の投与、そして安全性評価委員会のご承認を得て、その後の組入れ促進につなげたいと考えています。
発表機会を模索する学会およびシンポジウム(2026年)
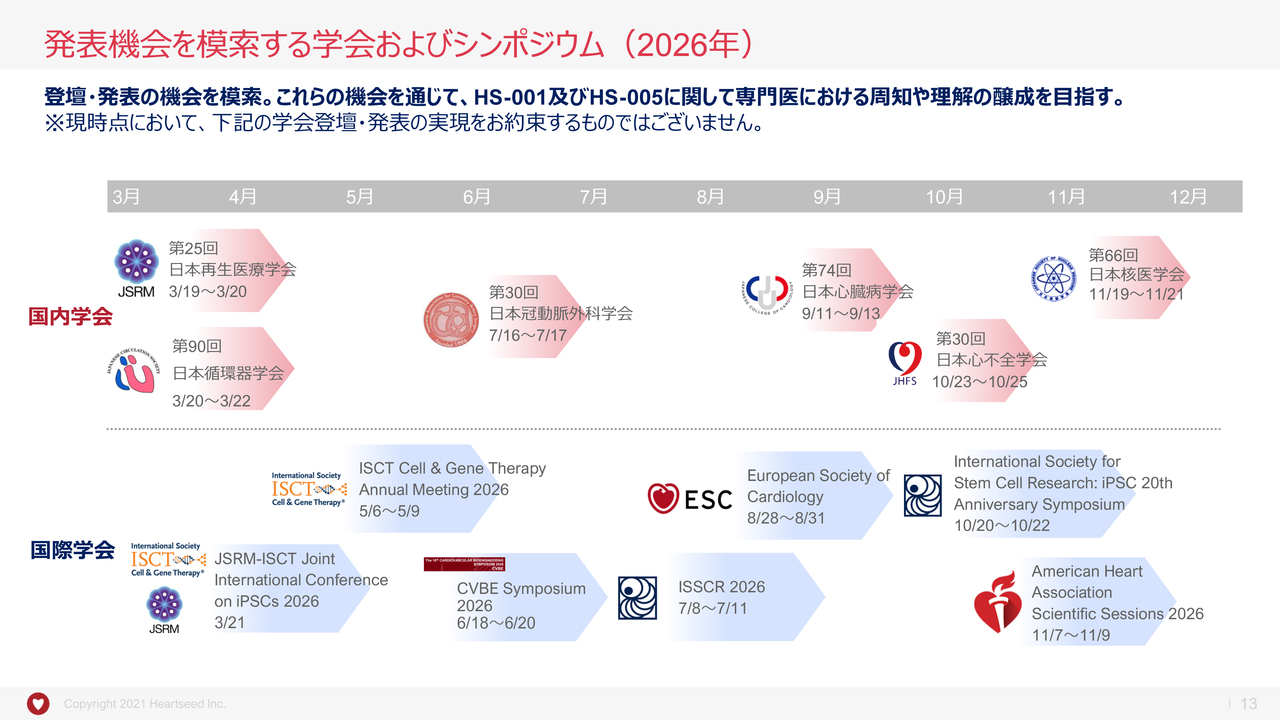
続きまして、今年に予定されている主な学会をお示ししています。治験施設の先生方による症例報告を期待するとともに、当社による臨床データの発表の場も模索していきたいと考えています。
これらの機会を通じて、「HS-001」や「HS-005」に関して、専門医における周知や理解の醸成を図っていきます。
グローバルな学術的プレゼンス向上に向けた着実な対外発表

それでは、ここで直近のトピックスについてお話します。
まずは治験データなどの対外発表について振り返りたいと思います。
まず、昨年9月から11月の間に、複数の国内学会において、治験施設の先生方より、初期データとともに症例報告をいただきながら、有効性やメカニズムの解析につながる多くの知見を頂戴しました。
そして、治験施設の国内発表をまとめたかたちで、米国AHAをはじめとする主要な国際学会において会社発表の機会を得ることができまして、順調な治験結果を示すともに実用化に向けて着実に前進している点などについてお話ししました。海外専門医のご理解とご関心が着実に醸成されつつあると肌で感じている次第です。
そして、こうした国際学会での発表の後、本年度のトピックとはなりますが、世界で最も権威ある国際学術シンポジウムの1つであるKeystone Symposiaより招聘を賜り、世界トップクラスの科学者に対し、当社の技術と臨床データを共有したとともに、未来の方向性を議論していきました。
このように、段階的に対外発表を重ねることで、グローバルにおける学術的プレゼンスの向上を着実に図っていきました。
世界的に権威ある国際会議にて、実用化を控えた企業として招聘されました。

続きまして、今お伝えした一連の発信の中でも、特に象徴的だったKeystone Symposiaについて、もう少しお話をしたいと思います。
ご存知の方も多いかと思いますが、Keystone Symposiaは生命科学分野において世界で最も権威ある国際学会の1つであり、世界からトップの科学者が招聘される非常に格式高い会です。
今回はiPS細胞発表から20周年という大きな節目に、ゆかりのある京都で開催され、山中伸弥先生がオーガナイザーを務められました。私は今回、社会実装に近い一企業として「臨床試験」に関するセッションにて登壇する機会をいただき、当社の技術や臨床データを中心に発表しました。
会場には、世界の再生医療を牽引する国内外の科学者だけでなく、一流の科学ジャーナル関係者やメディア等も情報収集をしに来ていました。そうした方々と直接、実用化に向けた展望などついて議論を交わせたことは、当社にとって大変意味のある登壇だったと考えています。
HS-005:2026年上期での投与開始に向け順調な進捗

最後に、カテーテル投与である「HS-005」の国内第I/II相試験である「EMERALD試験」についてお話します。
今回の治験には虚血性心疾患による重症心不全の患者さま7名と、拡張型心筋症による重症心不全の患者さま7名、合計14名の組入れを予定しています。
主要評価項目は投与後26週の安全性であり、副次評価項目は52週の安全性および26週と52週の有効性となります。
昨年11月に発表したとおり、PMDAへ提出した治験届の30日調査が完了し、国内での治験開始が正式に可能となっています。
現在複数の治験施設において、投与対象となる患者候補の探索に着手いただいたところです。
2026年上期中の1例目投与に向け、準備は大変順調に進んでいます。チーム一丸となって取り組んでいきますので、引き続きご注目いただけますと幸いです。
再生医療で心臓病治療の扉を開く

ご多忙の中、ご清聴、誠にありがとうございました。





