2026年3月24日に発表された、オンコリスバイオファーマ株式会社事業説明会の内容を書き起こしでお伝えします。
承認申請に向け ラストスパート!
浦田泰生氏(以下、浦田):代表取締役社長の浦田です。本日は、株主総会後に事業説明会にもご参加いただき、誠にありがとうございます。
これまでの株主総会後の事業説明会では、私がみなさまに事業の状況をご説明してきましたが、今回からは当社の執行役員が業務や事業の状況をより詳細にお話しする予定です。どうぞよろしくお願いします。
昨年の総会にご参加いただいた方は、スライドの「承認申請に向けラストスパート!!」という赤色の画像をご記憶かと思います。2025年は「OBP-301(以下、テロメライシン)」の承認申請に向けてラストスパートをかけ、年内に承認申請まで持ち込むことを目標に、社員一丸となって取り組んできました。
特にこの1年は、さまざまな出来事がありました。PMDAとの対応では、厳しい質問が寄せられたり、「重箱の隅をつつく」とは言いませんが、非常に細かな点について確認を求められることもありました。
こうした課題を乗り越え、昨年12月15日になんとか承認申請に持ち込むことができたのは、みなさまのご支援のおかげです。あらためて感謝します。また、社員一同の努力の成果でもあります。
2026年

2025年のラストスパートの後となる2026年について、お話しします。私が2004年に当社を創業し、すでに22年が経過しました。このため、創業当時から開発を進めてきたことについてお話しします。
腫瘍溶解ウイルス「テロメライシン」は承認申請を経て承認され、今後薬価が設定されることで、日本のがん治療を担う病院での実際の使用が可能となります。すなわち、2026年は大きな変化を遂げる年となります。そのような意味で、今年は当社にとって、スライドに記載されているように「テロメライシン」の集大成の1年になると考えています。
また、株主総会でご質問があったように、「創薬ベンチャー企業」から製造販売が可能な「製薬企業」への転換を実現するための第一歩を踏み出す年になると考えています。
これからのオンコリス

この第一歩を踏み出した後に、当社がどのような会社になっていくのかについてご説明します。これまでは開発についてお話ししてきましたが、来年の今頃には「テロメライシン」の売上や効能追加、あるいは「OBP-702」といった第2世代の「テロメライシン」、さらには今後どのような薬になっていくのかについても問われるような会社へ成長していくと考えています。
なお、現在ベルギーの会社に製造を委託しているウイルスについても、製薬企業として自社で製造できる体制を、2035年よりも早い段階で整えたいと考えています。また、将来的には自社でセールス機能も持つような企業を目指していきたいと思います。
“Next Door” ~新たな展開へ~

それらを踏まえて私が今年社員に提示した合言葉は「“Next Door” ~新たな展開へ~」です。「当社も新たな展開に向かっていこう」、「これまでの創薬ベンチャーとは異なり、製造販売ができる会社にしていこう」とお話ししました。「新しい扉を開いていく」という意気込みを込めて、モニュメントではありませんが、スライドのような絵にしています。
2025年~今日までの主な活動

今日までの主な活動をご報告します。1つ目は、PMDAとの話し合いについてです。社長コラムなどで詳細をお伝えしたかったのですが、非常に秘匿性の高い内容が多く含まれていたため、ご報告が難しい状況でした。
例えば、品質や製造に関する点についても、当社のノウハウに深く関わる部分があり、十分にお話しすることができませんでした。本日は後ほど執行役員からお話する予定です。
当社が取り組んできた中で苦労しつつも成し遂げた事柄として、2つ目に挙げられるものがヘノジェン社に関する取り組みです。ベルギーのヘノジェン社はウイルスを製造している会社であり、施設や関連施設を監査しました。それ以外にも、例えば「テロメライシン」を入れるガラス瓶を製造する会社や、蓋を閉めるゴム栓を製造する会社なども含めて、非常に綿密な監査を実施し、製品が適切に作られていることをPMDAに証明する取り組みを行いました。
3つ目は、信頼性保証調査です。これは今年に入ってからの取り組みで、当社が臨床試験を適切に実施しているかについて、PMDAが確認を進めています。
具体的には、全国17施設で行われた「テロメライシン」の臨床試験について、適切な体制で試験を実施しているのかについて、PMDA職員が当社および臨床試験施設の監査と膨大な書類のチェックを行いました。
みなさまもご存じのように、「テロメライシン」は2019年から約3年にわたり中外製薬が開発を進めてきた経緯があります。このため、中外製薬から当社に権利が戻ってきた際の書類のやり取りなど細部にわたる内容も非常に厳しくチェックされました。これらもすべて合格したと認識しています。
4つ目は、サプライチェーンの構築です。後ほど詳細をご説明しますが、現在はベルギーでウイルスを製造し、瓶詰めを行って日本国内に空輸しています。日本ではさらに箱詰めを行い、日本語表記の「テロメライシン」という箱に梱包し、マイナス80度で臨床施設に輸送しています。
このご説明では簡単そうに聞こえるかもしれませんが、非常に大変な作業です。ロジスティックの経験がないため、専門家を招いてようやくサプライチェーンの全貌が見える状況となってきました。
岡山大学消化器外科学 藤原俊義教授 退官祝賀会2026.3.22

3月22日、当社の創業メンバーであり、岡山大学消化器外科学の藤原俊義教授の退官記念祝賀会が開催されました。創業当時、藤原教授は助教でしたが、2010年から岡山大学第一外科の教授を務め、先日その44年のご功績を称えられました。なお、私も祝賀の席で祝辞を述べました。
藤原教授は先進的な医療手法「テロメライシン」の考案者であり、これまでの22年間、当社と二人三脚で共に歩んでこられました。今後は四国の病院の院長として新たな地でご活躍されますが、当社との絆と共同研究の継続を堅持します。
なお、岡山大学第一外科は約500人規模の関連者で構成される非常に大きな組織であり、祝賀会当日も大変盛大に執り行われました。
2025年12月末のパイプラインの状況
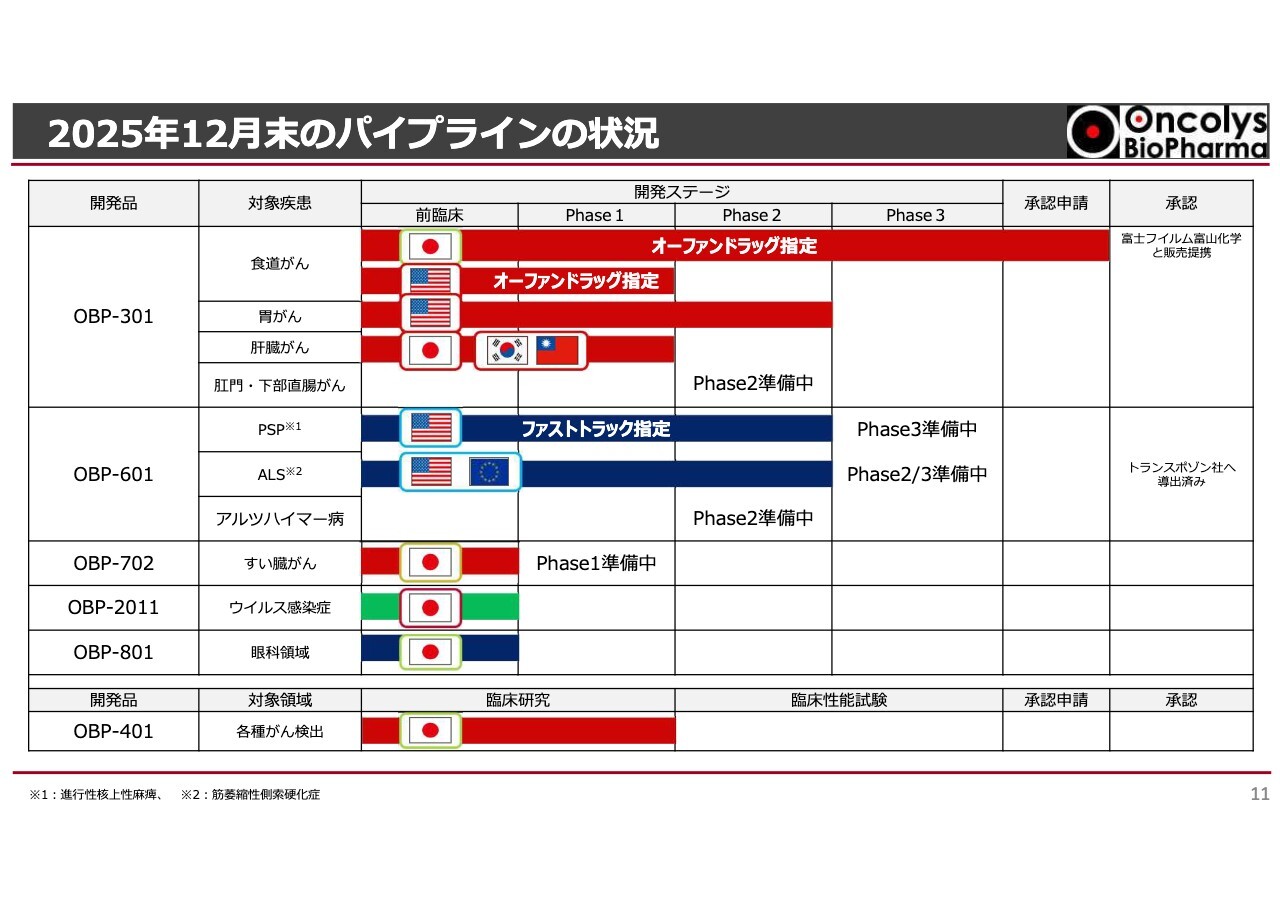
当社のパイプラインの状況についてです。詳しくは後ほどお話ししますが、「テロメライシン」はスライドの赤色のラインになります。日本では承認申請中、アメリカでは胃がんの臨床試験が進行中です。
また、アメリカでは化学放射線療法との併用試験がいったん終了したところです。この点についても後ほど詳しくお話しします。
神経難病に対する「OBP-601」については、青色のラインでお示ししています。ファストトラックの指定や優先審査を受ける状況にあり、いよいよアルツハイマー病の治験が始まる段階にきています。こちらも後ほど詳しくお話しします。
「2025年にご期待頂きたい事項」の結果

スライドは2025年の株主総会でみなさまに提示したものです。全部で8項目あり、1番目は先駆け総合評価相談を開始すること、2番目は国内承認申請を行うこと、3番目は国内オーファン申請を行うこと、4番目は再生医療等製品販売業の業許可を取得すること、5番目は最終製品や製剤で示した製品が1年間安定していることを試験でクリアすること、6番目は「テロメライシン」を内視鏡で投与するという、当社にとって非常に心強い特許を取得できるかどうかについてお約束しました。
「テロメライシン」 に関する1番目から6番目については、当社が自力でできることに関して、みなさまにしっかりお約束を果たせたのではないかと考えています。
一方、「OBP-601(Censavudine)」に関しては、7番目にあるアメリカで進行中の神経難病における最終臨床試験の開始とマイルストーンの受領、8番目にあるアルツハイマー病での試験開始を計画していたものの、残念ながら未達成となりました。
「OBP-601(Censavudine)」については、アメリカのTransposon社に完全ライセンスアウトしています。このため、開発に口出しはできるものの、実際に手を出すことはできない状況です。
「もっと早く開発を進めてほしい」との要望を出してはいますが、昨年トランプ政権が製薬メーカーに対して非常に大きなプレッシャーをかける発表を行ったことを背景に、大手製薬メーカーが儲かる領域、例えば肥満、精神病、抗うつ剤などに資金を集中しており、アルツハイマー病やALS(筋萎縮性側索硬化症)などの神経難病にはなかなか資金が回らないという現状があります。そのため、現在、Transposon社が資金調達を進めているところです。
テロメライシンのメカニズム
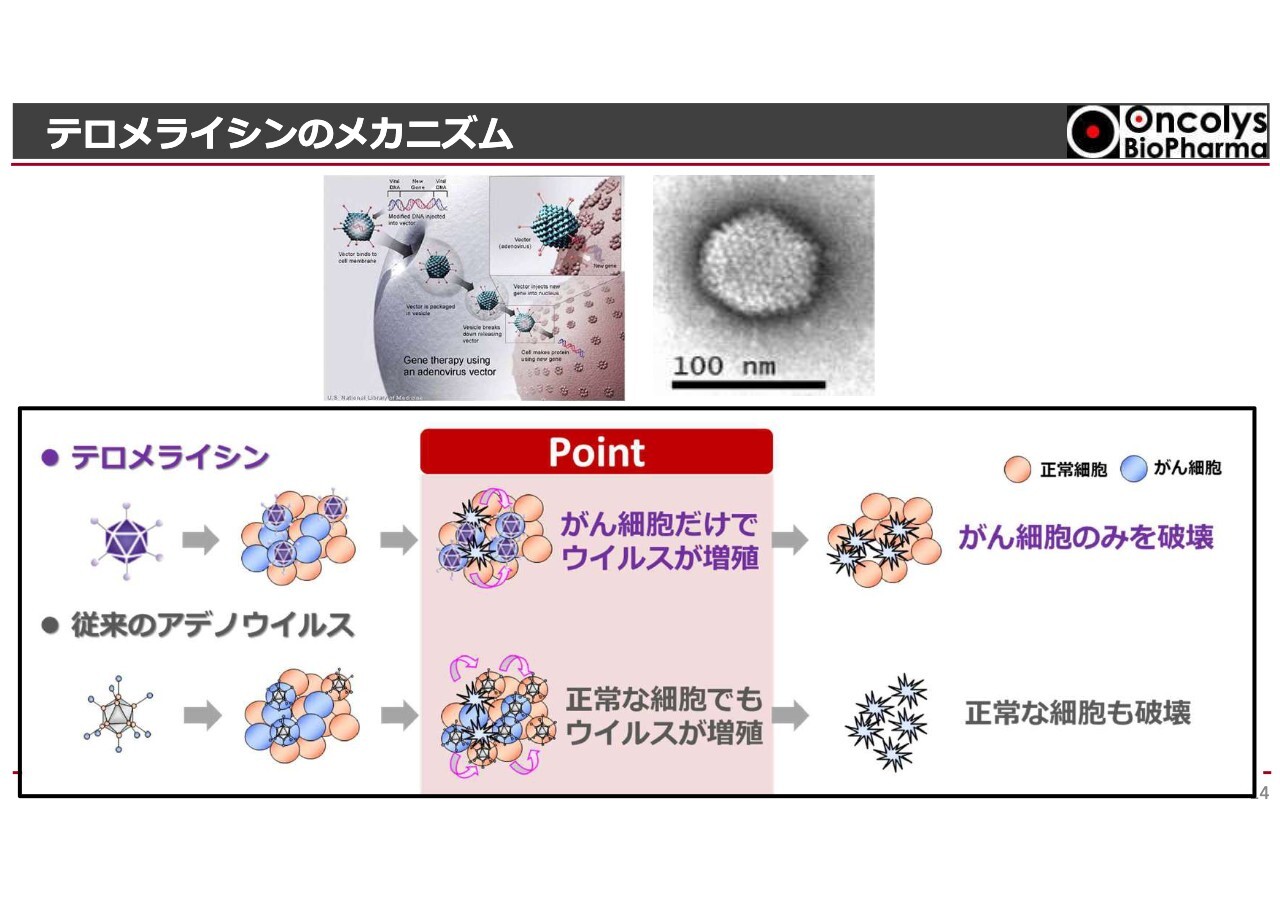
株主総会や事業説明会に初めてお越しの方もいらっしゃるかもしれないので、「テロメライシン」のメカニズムについてご説明します。
「テロメライシン」はアデノウイルスという、扁桃腺炎を引き起こすウイルスをベースにしています。ただし、インフルエンザや新型コロナウイルスのように感染すると致死的な状況をもたらすウイルスではありません。風邪のような症状やのどの痛みを引き起こすウイルスです。
なによりもまず、安全性が確保できるウイルスであることが大切です。他にもさまざまなウイルスがありましたが、アデノウイルスを用いることで、がん細胞に感染し、そこで増殖させることができます。
一方で、このウイルスは正常細胞にも感染しますが、扁桃腺炎を引き起こすなどの悪影響はほとんど生じないように設計されています。このウイルスはがん細胞のみで増殖し、がん細胞を破壊するという特性を持ちます。こうした性質はみなさまも十分ご存じかと思います。
このウイルスを基にした「テロメライシン」は、創業以来、藤原教授とともにどのように開発するのかさまざまな議論を重ねてきました。実験的には、どのようながんにも効果があります。ただし、臨床においては状況が異なり、マーケット規模の大きい肺がんや大腸がんでは投与が難しいため、これらのがんを狙うことは現実的ではないと当初より判断していました。
業界ではアンメット・メディカル・ニーズと呼ばれている、非常に重要な重い病気だが治療法や治療薬がない領域で戦っていこうと考えています。また、大企業がやらない、患者数が少ない領域、さらには大企業が敬遠するウイルス領域で戦ってきたという歴史があります。
世界のがんウイルス療法の開発状況
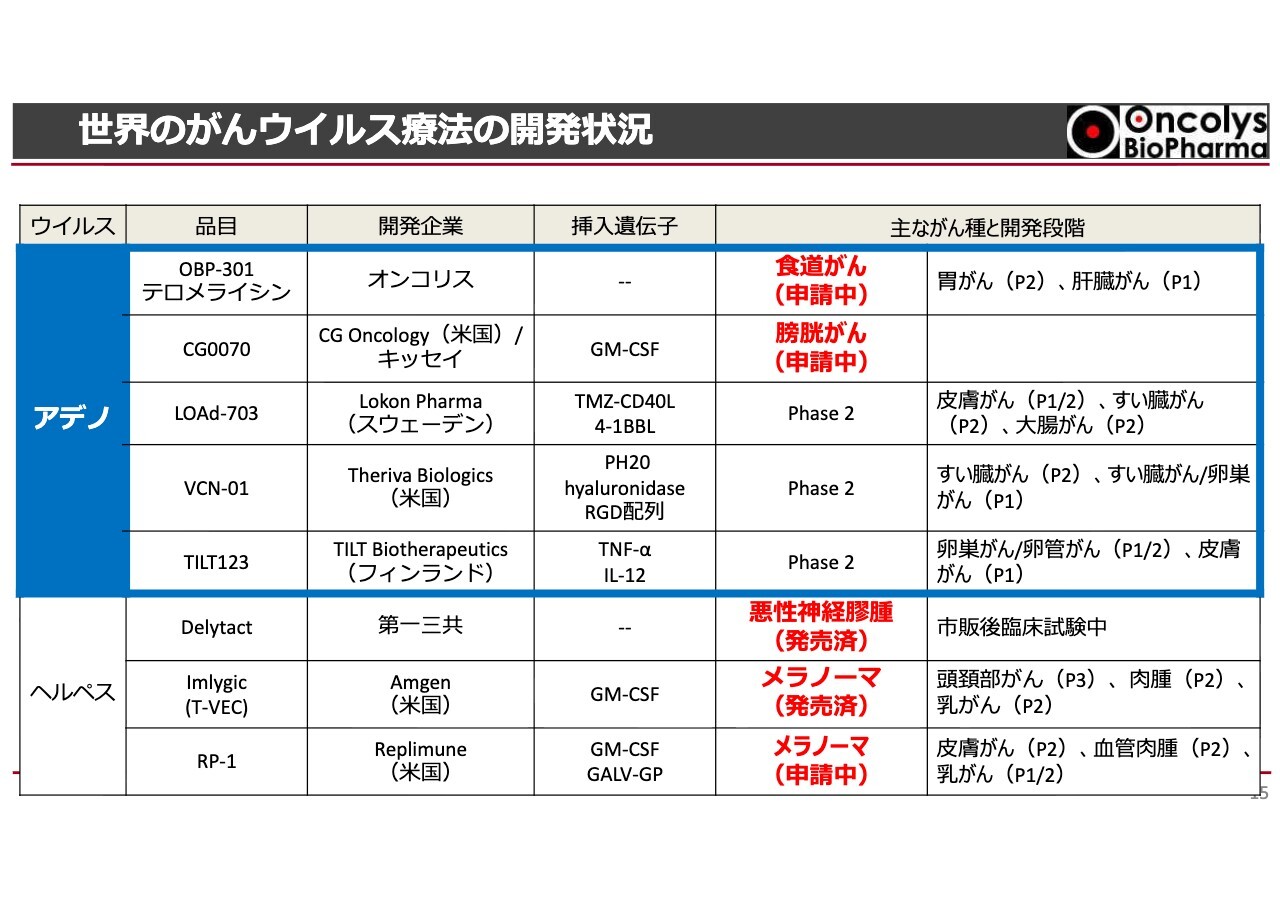
現在の世界的な競合状況についてご説明します。スライドの青色で囲んだ部分が、アデノウイルスの競合状況をお示ししています。その下には、ヘルペスウイルスが記載されています。
ヘルペスウイルスについては、脳腫瘍の薬として第一三共から「デリタクト」が発売されています。「デリタクト」はいわゆる条件付き承認を受けており、全例のデータを収集する義務を伴う試験を実施しなければならない状況で現在販売されています。販売開始後、7年間の期間を経て再審査が行われる予定であり、その期限まであと2年残っていると考えています。
アメリカではヘルペスウイルスを利用した治療法として、メラノーマ(悪性黒色腫)に対する開発が進められており、Replimune社のウイルスがメラノーマで申請中という状況です。なお、食道がんに対して取り組んでいるのは当社のみとなっています。
一方、アデノウイルスについては、最上段に記載している当社以外に、「CG0070」というウイルスを開発しているCG Oncology社とキッセイ薬品工業が協力し、膀胱がんの臨床試験を実施しています。この試験は現在アメリカで承認申請が行われていますが、日本国内での動きはまだ見られません。
その他、スウェーデンのLokon Pharma社、アメリカのTheriva Biologics社、フィンランドのTILT Biotherapeutics社といった企業が、それぞれPhase2を進めています。
スライド右側には、皮膚がんや膵臓がん、卵巣がんといった適応症をお示ししていますが、当社のように食道がんを対象にしている企業は存在しません。私が調べた範囲では、食道がんの局所治療薬は世界中で当社の「テロメライシン」だけであり、承認されれば世界で初めての食道がん局所治療薬となると思います。さらに、日本国内においてアデノウイルスを用いた腫瘍溶解ウイルス製品が承認されるのも、初めてとなる可能性があります。
OBP101JP試験の有効性
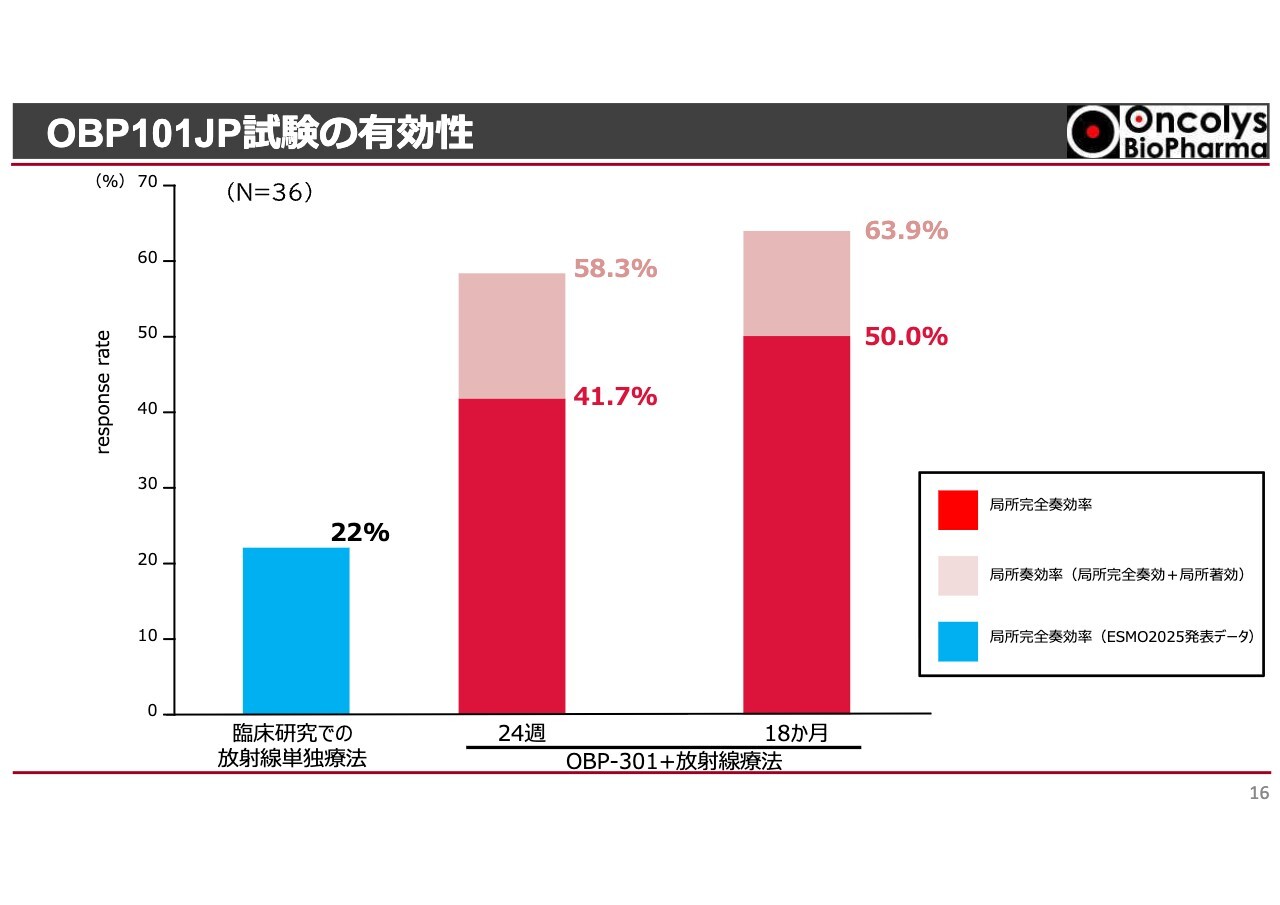
スライドは、今回PMDAに提出した資料になります。治療開始から24週後についてお示ししています。中央の棒グラフにあるとおり、41パーセントの方で完全にがんが消えました。58.3パーセントの方には一部が残存しているものの、合わせて58.3パーセントの方に効果がありました。
さらに治療開始から1年が経過すると、治療効果がさらに向上し、ステージ2およびステージ3の食道がん患者さまの50パーセントで完全にがんが消失したという結果が得られました。
後ほど執行役員がご説明しますが、こうした患者さまの生命予後については、少なくとも1年半の間は再発しなかったことが確認されています。いわゆるCR(Complete Response:完全奏効)という状態が達成されています。
さらにいえば、患者さまががんという状況から完全に解放された状態を当社では「キュア」と呼んでいますが、そうした状況が形成されたのではないかと先生方も評価しています。
通常、肺がんや大腸がん、乳がんにおいて、抗がん剤を使用した結果として、局所のがんが完全に消失する割合は10パーセントから15パーセント、多くても20パーセントほどとされています。このような状況下で、当社は50パーセントという高い結果を得られたことになります。
スライド左側の22パーセントという数字は、今回の臨床試験を実施した施設の先生方に依頼し、過去10年間にわたって今回の試験と同じ症例を集めていただいた結果です。その結果、放射線単独療法では22パーセント程度にとどまってしまうことがわかりました。
これに「テロメライシン」を上乗せすると、40パーセントから50パーセントに効果が上がるという結果が得られました。PMDAは当初疑問を持っていたものの、治験施設の先生方がPMDAにデータの重要性を強く主張してくださったことで、PMDAの考え方も途中から変わりました。
その後はPMDA側からも迅速さを求める声が上がるようになり、早急に照会事項に対する回答を当社から出すよう促されました。このような状況の中、当社も土日や深夜を問わず必死に回答書を作成するかたちで対応するなど、緊張感の中で業務が進められました。
このようにして「臨床試験について確認できました」という段階まで進みました。おそらく今月中に審査が終了し、いよいよ厚生労働省の評価に入る状況となっています。
海外臨床試験

アメリカの状況についてご説明します。これまで何度もお伝えしているとおり、大きな進捗はないものの、少しずつ動いています。
1つ目は、食道がんの化学放射線療法(CRT)の併用試験についてです。この試験は、ニューヨークのトップクラスのがん施設であるメモリアル・スローン・ケタリングがんセンターで実施された「テロメライシン」を使用したPhase1試験です。
すでにIRでご報告しているとおり、この試験では全例で局所がなくなったという結果が出ています。ただし、1年生存率は60パーセントという結果でした。なお、1年生存率とは、例えば合併症で亡くなった方や、他の原因で亡くなった方も含まれている数値です。
局所再発がなかった症例は13例中12例であり、92パーセントという非常に良い結果が得られました。現在、この結果について論文を投稿中です。
現在は、メモリアル・スローン・ケタリングがんセンターの先生方が試験計画を立てています。ただし、今回は13例という少数例の試験でしたが、次回は150例から200例規模の大きな治験となるため、資金がかなり必要となります。資金が獲得できれば、国際臨床試験としてさらに進めることが可能な状況にあります。
2つ目は、胃がん治療における「ペムブロリズマブ」の併用試験についてです。これは、MSD社が協力して進める免疫チェックポイント阻害剤に関連する治験です。
「ペムブロリズマブ」では、胃がん治療で免疫チェックポイント阻害剤を使用したものの完全に効果がなくなったケースが対象となります。ファーストライン治療では約15パーセントの患者さまが生存可能となりましたが、これは手術ができない患者の場合です。約85パーセントの患者さまは治療効果が見られず再発してしまう状況です。
この治験では、再発した患者に対して免疫チェックポイント阻害剤を継続しつつ、「テロメライシン」で胃がんの局所に追加治療を行うことで、どのような効果が得られるのかを検証しています。
実際、昨年から一昨年にかけて行われた治験では、免疫チェックポイント阻害剤単独では効果がなくなった患者さまの中に、脳への転移腫瘍が消失した例が確認されました。この結果を受けて試験を拡大し臨床試験が進められており、目標とする13例のうち12例の投与がすでに完了しています。
この試験は生存率の推移を確認する試験でもあるため、最終的な結果が出るまでにはもう少し時間がかかると考えられます。
テロメライシンは、

「テロメライシン」は世界初の食道がんに対する局所治療薬となる可能性が高まっています。さらに、世界初の腫瘍溶解アデノウイルス製剤になる可能性も高まっています。
局所の完全奏効率は50パーセントと非常に高い割合を示しています。主な副作用はスライドに記載のとおり、発熱や軽い神経のしびれ程度であり、注射後の一晩ほどで収まります。また、リンパ球数が低下する副作用も見られるものの、痛みなどは伴わず、全体的な免疫機能は保持されたままリンパ球数のみが一時的に減少する状況です。
これまでの抗がん剤とはまったく異なり、副作用が非常に軽微であることから、9時間にも及ぶような食道がん手術を行わずに治療が可能となる可能性があります。化学療法による非常に苦しい副作用に悩むことなく、日本の医療現場で治療を受けられる可能性が非常に高まってきています。
一方、ウイルスが体内に入ることで何が起こるかわからないという理由から、病院に最低1週間ほど入院していただく治験を実施していました。ただし、実際に患者さまの血液や喀痰などを検査する中で、尿や糞便などをさまざまに調べた結果、投与した翌日には、ほとんどのウイルスががんの局所でのみ増殖しており、全身にはあまり影響を及ぼさないことが判明しました。
これにより、仮にウイルスが体内に残っていたとしても、マスクを着用すれば通院での治療が可能となります。また、治療後にけがをして出血した場合も、絆創膏を貼り、外す際にはその絆創膏をビニール袋に入れて家庭用のキッチンハイターを散布し、通常のゴミ箱に捨てるだけで問題ないことが確認されています。
治験時には内視鏡室を完全に目張りし、医師も厳重に防御装備を着用して治験を実施していましたが、現在ではそのような厳重な対応は不要となりました。内視鏡で「テロメライシン」を投与することは、新型コロナウイルスの感染予防対策で世界的に行われてきた方法と同程度のやり方で十分であり、投与を受けたその日に自宅に帰れるという状況が、実現しつつあります。これは非常に大きな進歩だと思います。
また、高齢者にも非常にやさしい治療になるため、手術が困難な方にとっても福音となると考えています。
このように、「テロメライシン」は日本の食道がん治療の現場に大きな改革をもたらす薬になると期待されています。
テロメライシンの発売に向けて
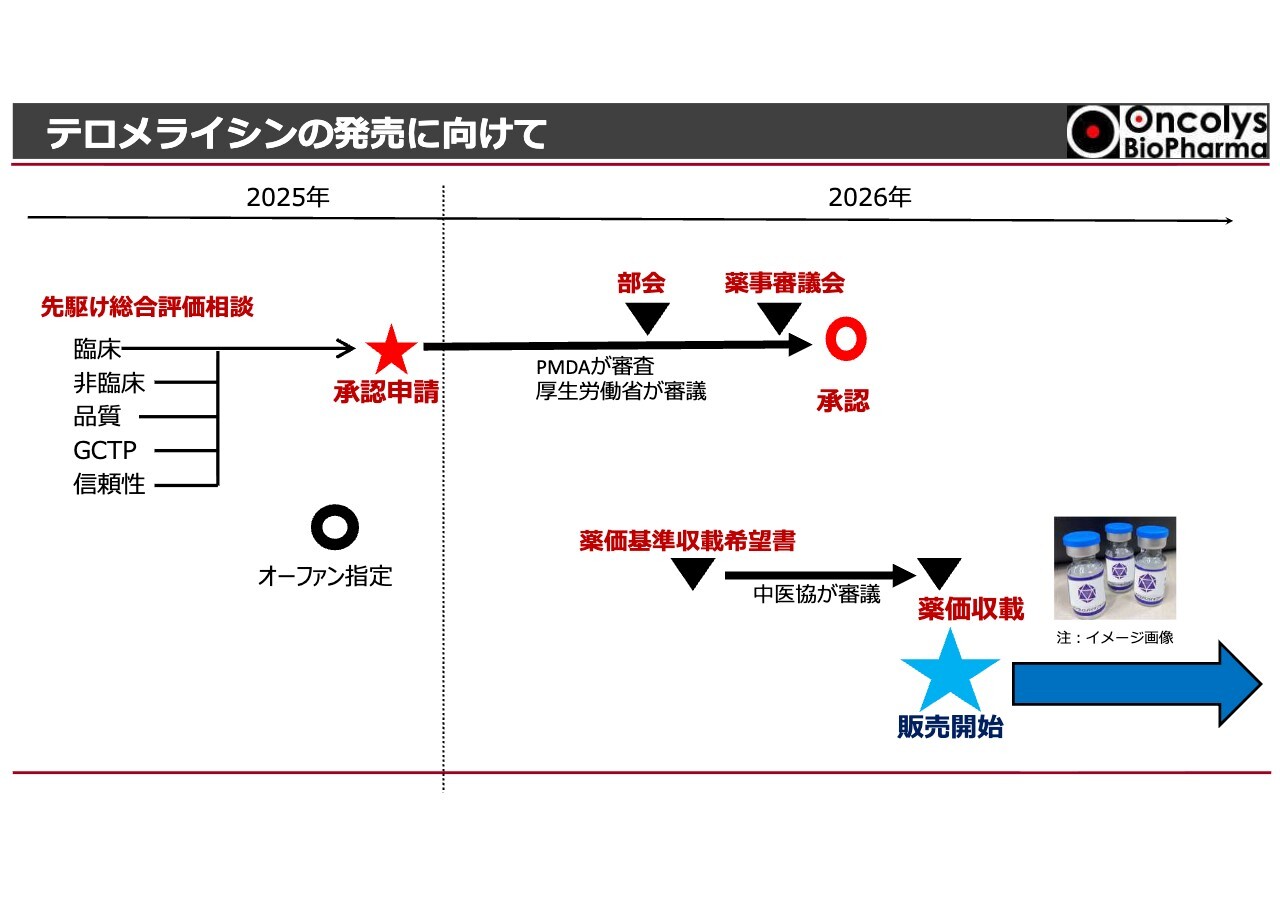
おそらく今月中にPMDAの審査が終了する見込みです。審査が終了すると、厚生労働省に移り、専門部会で審査が開始されます。今年の5月から7月頃に薬事審議会で審査が行われ、問題がなければ正式に承認されると考えています。
当社は条件のつかない通常承認を目指しています。この現状については、PMDAとのこれまでの対話において齟齬がなく、PMDAから懸念が示されたこともありません。
逆に、条件付き承認となった場合、たとえ承認が得られてもその後臨床試験を実施しなければならず、多額の費用が発生します。販売で得た収益を再度臨床試験に充てる必要が生じる場合もありますが、このような状況を避けることはできると考えています。
なお、製造面においてウイルス製造が安定供給できない場合には、条件付き承認となる可能性があります。しかし、現段階では安定供給体制が準備されており、製剤の安定性も高いと考えています。すでに1年半の安定性に関するデータは揃っており、年内には2年間の安定データが得られる見込みです。このような状況のもとで、薬を販売していきたいと考えています。
さらに、当社は薬価の設定について慎重に検討しています。スライド下部の「薬価基準収載希望書」にも示されているとおり、薬価は経営において非常に重要な要素と捉えており、高薬価の取得を目指すことが当社の経営方針にとって重要だと考えています。もちろん、できるだけ多くの方々にお使いいただける薬を目指していますが、これまでの投資を回収する観点からも、可能な限り高い薬価の設定を目指したいと考えています。
なお、薬価については後ほどお話しします。
当社は、食道がんの治療において、手術や抗がん剤治療ができない患者さまに対して「テロメライシン」を用い、完全治癒を目指しています。また、もう少し幅広い患者層として、抗がん剤治療後の患者に投与して「テロメライシン」で完全治癒を目指せる薬へと展開することや、早期の患者さまにも使えるようにしたいと考えています。
今後については、今回の許可に基づいて厚生労働省と協議しながら、対象となる患者層を拡大できるかが1つの課題となってきます。現在、ステージ2やステージ3の患者さまを対象に臨床試験を実施していますが、ステージ1やステージ0.5の患者にも適用できるかどうかが今後の焦点になると考えています。
食道がん領域でブランド確立

当社は食道がんという分野で取り組んできたので、今後も食道がんのスペシャリティファーマを目指していきたいと考えています。
「食道がん局所療法研究会」を発足し、食道がんにおいてさらに幅広く使用できるような臨床試験を組んでいきたいと考えています。
効能追加の計画
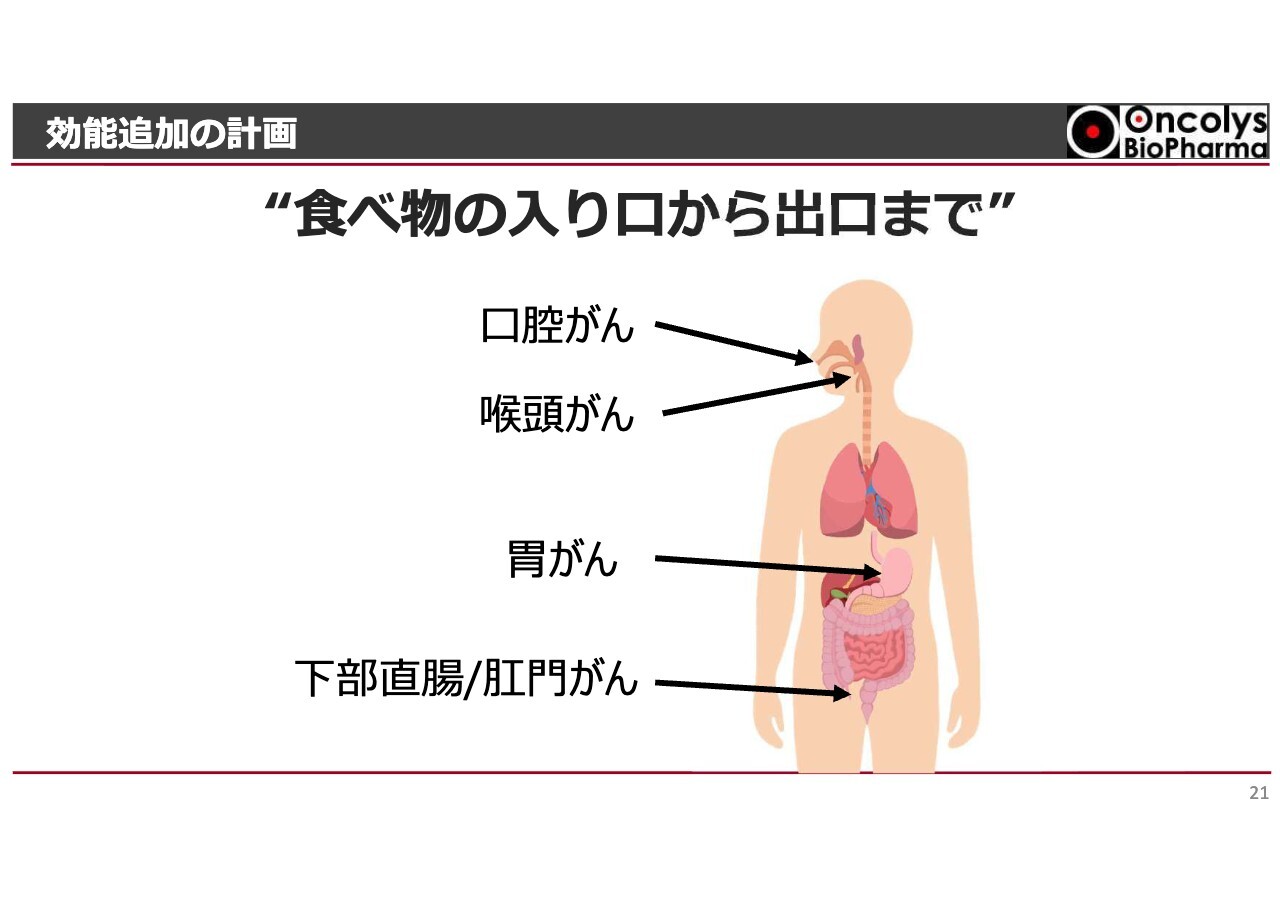
効能追加については、後ほど執行役員からお話しします。
高薬価戦略

適正な薬価についてお話しします。「適正な薬価」と「高薬価」は異なる言葉ですが、当社としては「当社にとって適正な薬価」を目指していきたいと考えています。
通常承認を狙う場合についてご説明すると、例えばノバルティス社がアメリカで遺伝子治療薬「ゾルデンスマ」の承認を取得しています。この治療法は非常に高額で、アメリカでは1億円を超える治療費が必要です。ただし、日本では再生医療等製品に該当するかたちで通常承認を取得しています。
また、みなさまもニュースでご覧になったことがあるかもしれませんが、iPS細胞を用いた薬や、細胞治療で外傷性脳損傷に関する承認を取得した薬も存在します。これらの会社はすべて条件付き承認を受けています。
そのような意味では、ノバルティス社の遺伝子治療以来、もし通常承認を取得できれば、それに準じた通常承認という扱いになると考えています。
業界においてこれは非常に意義のあることであり、当社としても追加の臨床試験を行わなくても済むという理由から、通常承認にこだわっています。
また、薬価を設定する上で重要なポイントとして、先駆け加算が挙げられます。これは日本で先駆けて許可を取得することに対するものであり、さらにオーファン加算もあります。オーファンとは「みなしご」という意味であり、みなしご病という表現を用います。当社が現在食道がんで取得しているものは、手術ができない患者さまを対象にしたもので、オーファン疾患、すなわち治療薬がない領域に該当しています。このような場合も加算がつく可能性があります。
さらに、今回の50パーセントの完全治癒を達成したという事実は非常に有効であり、副作用が少ない点でも有用であると考えています。このような薬価に対する加算を徹底的に向上させる取り組みを進めていきたいと考えています。
薬価を決定する際には、原価の開示率、すなわち「テロメライシン」を工場で製造する際の実際のコストや原料費がどの程度かを開示する必要があります。現在、実際に薬を製造しているベルギーの会社から当社への情報提供は受けられていませんが、原価に関しては厚生労働省がベルギーの会社と適切にやり取りを行えるような仕組みを整備しています。このようにして開示率が向上することで、適正な薬価を得られると考えています。
発売開始の準備

発売開始の準備として、スライドに挙げている医療関係者向け資料や患者向け資料があります。
当社の担当者が作成した医療関係者向け資料は、50ページから60ページほどのガイドラインとなっています。この資料には、私がこの22年間に携わってきた非臨床試験、品質試験、臨床試験など、多岐にわたる内容が非常に平易な言葉で記載されています。また、医療関係者が「テロメライシン」という製品をどのように注射針に取り付け、内視鏡でどのように投与するかについても明確に記載されています。
このような資料が完成することに、私は感無量です。創業当時はここまでたどり着けるかどうか明確な見通しがつかなかったものの、実際に出来上がった医療関係者向けの資料や、患者向けに非常にわかりやすい言葉で作成された資料を目にし、感慨深いものがあります。ここまで来られたことを、心から感謝しています。
テロメライシンの成長戦略

「テロメライシン」の成長戦略についてです。さまざまな取り組みを進めていますが、最終的には売上が伴わなければみなさまにご納得いただけない状況です。このため、一定の薬価が設定され、効能や効果の追加がなされることで、食道がん市場においてしっかりとブランディングを行い、シェアを拡大していく方針です。
これまで「50億円売れます。100億円売れます」といったお話もしてきましたが、薬価が決まらないとなかなか詳細をお伝えすることができません。ただし、先ほどお伝えした第一三共が提供するヘルペスウイルスを用いた脳腫瘍治療薬には、1瓶あたり140万円という薬価が設定されています。これが当社の「テロメライシン」にどのように適用されるかは現時点ではわかりませんが、それを上回る薬価を主張していきたいと考えています。
そのような薬価が実現すれば、患者さまの支持を得ることやブランディング、さらにシェア拡大を計画的に進めることで、早期に黒字化を達成できる可能性が高まると考えています。
トランスポゾン社の今後の展開
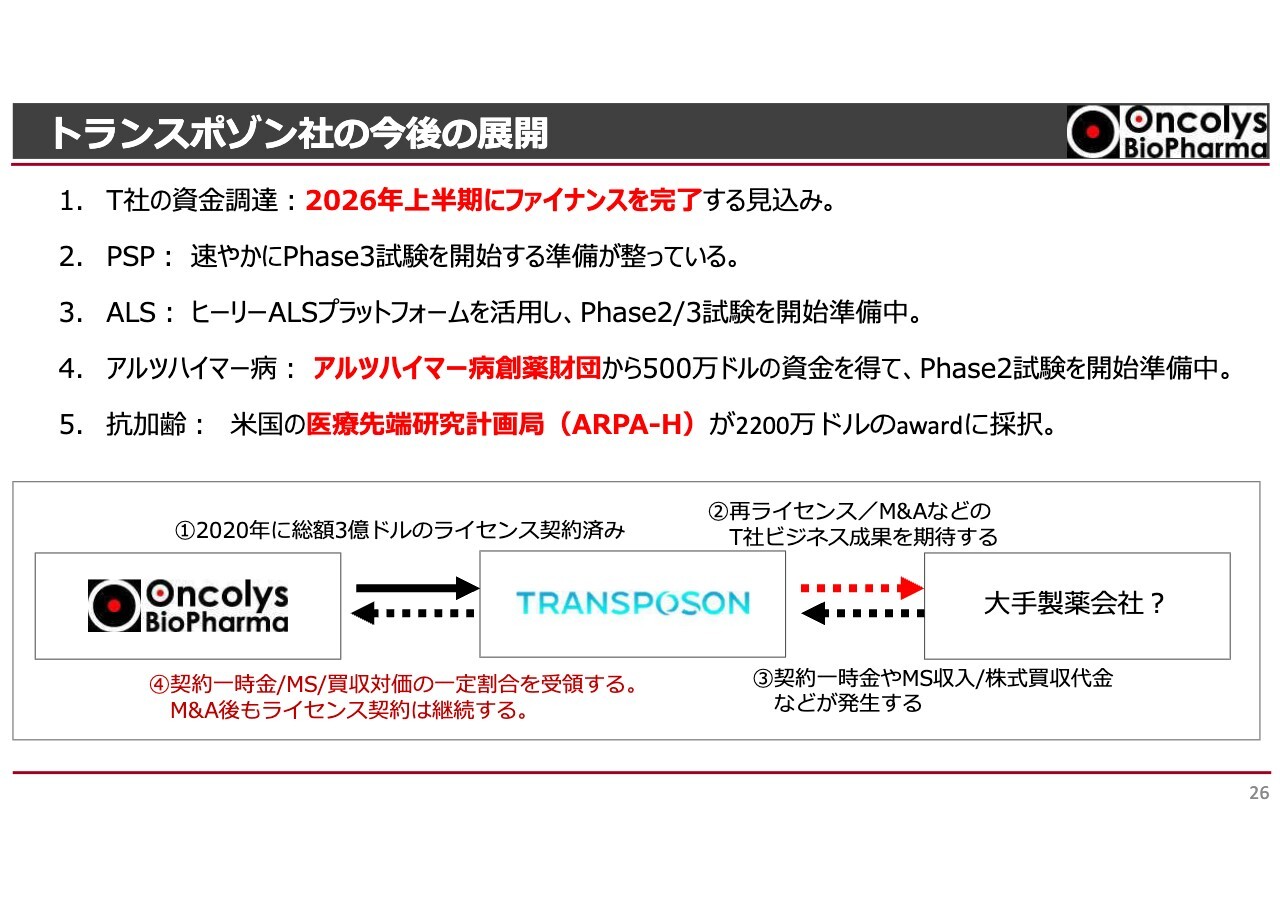
最後に、株主のみなさまが特に気にかけている「OBP-601」の状況についてです。Transposon社とは昨今さまざまな話し合いを進めており、昨年まで臨床試験の結果をご報告してきました。
スライド2番目に掲載しているPSPは、進行性核上性麻痺という難病です。パーキンソン病によく似ていますが、認知機能や運動機能にも障害を及ぼします。「OBP-601」はPSPに対して神経の変性をある程度防ぐ効果があるという結果が得られています。
3番目に記載しているとおり、ALSに対しても一定の効果が確認されており、アメリカでALS治療薬の臨床試験を実施する「HEALEY ALS Platform Trial」にも採択されています。
しかしながら、資金調達に関しては厳しい状況が続いています。トランプ政権下でバイオ企業の上場数が著しく減少したことに伴い、このプロジェクトの進捗も思うように進まない状況が続いているようです。
4番目のアルツハイマー病については、すでにみなさまにご報告したとおり、アメリカのアルツハイマー病の創薬財団から500万ドルの資金を獲得しており、臨床試験計画がまとまりました。資金の調達が完了すれば、この試験を開始することが可能となります。
5番目の「抗加齢」については、当社も予想していなかったものになります。アメリカの医療先端研究計画局(ARPA-H)が、レトロトランスポゾンを阻害するLINE-1阻害剤「OBP-601」に対して、健やかな加齢を促す可能性を評価し、この薬の臨床試験に関連して2,200万ドルの研究費を提供しました。
このように周辺からのニュースが多く寄せられる一方で、Transposon社の資金調達に関しては、この1年間ほとんど動きがありませんでした。しかしながら、直近では当上期中に資金調達が完了し、臨床試験を開始する可能性が非常に高まっていると報告を受けています。
これが実現すれば、臨床試験が具体的に動き出すことになりますが、もう1つ重要な点として、大手製薬メーカーとのディールが挙げられます。私自身もこの件に非常に注目しています。
こちらも、「ALSにとても興味があるけど、他はちょっと興味ない」「全部はお金がかかりすぎるから、他のものでやりたい」「アルツハイマー病だけに興味がある」など、いまだ利害が一致する段階には至っていません。現在Transposon社は「OBP-601(Censavudine)」の価値を最大限に高め、大きなディールを実現しようと取り組んでいる状況です。
私としても大きなディールの実現を強く期待しており、臨床試験を早急に開始し、その成果を基に大きなディールにつなげるよう、Transposon社に申し入れています。
Transposon社は少なからず政治的な影響を受ける可能性も考慮しつつ、資金調達が具体化してきているため、年内にはいろいろなご報告ができるのではないかと考えています。
以上、Transposon社の現状についてのご報告となります。
「2026年にご期待頂きたい事項」

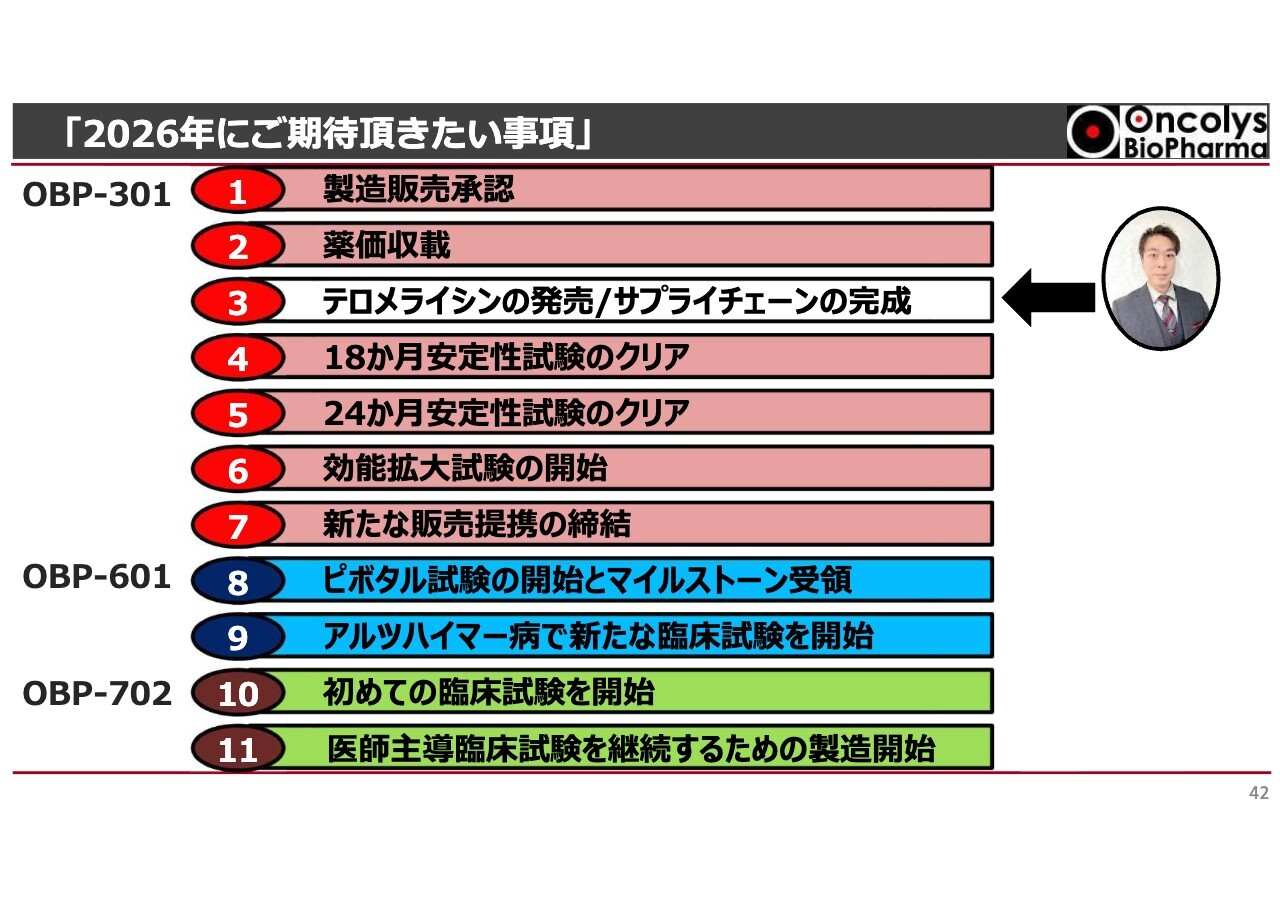
今年注目していただきたいポイントは、スライドの11項目になります。「テロメライシン」については製造販売承認を確実に取得し、薬価収載についても適切な薬価として収載されるよう全力を尽くしていきます。「テロメライシン」の発売にあたり、サプライチェーンを確実に整備し、漏れのない、かつ過剰在庫を抱えることのない体制を構築していきたいと考えています。
4番目と5番目の最終製品の安定性試験のうち、4番目については今年2月に18ヶ月間安定であるという結果が確認されました。5番目については、今年の秋頃に24ヶ月間、すなわち2年間の安定性データを得ることで、市場での安定供給の確実性が一層高まる見込みです。6番目の「テロメライシン」の効能拡大試験については、2026年に開始する予定です。7番目として、新たな販売提携先を締結します。こちらは海外に関する内容で、後ほど詳しくお話しします。
「OBP-601」については、昨年と同様にピボタル試験の開始やマイルストーンの受領、さらにアルツハイマー病における臨床試験の開始を、Transposon社に確実に進めていただきたいと考えています。
第2世代の「テロメライシン」である「OBP-702」については、年内に臨床試験を開始するとともに、今後のGMP製造のプロジェクトも立ち上げていきたいと考えています。
以上が、2026年に向けてご期待いただきたい事項です。
このように、当社にはまだ多くの課題が残されており、現時点では「テロメライシン」の承認と発売に全力で取り組んでいる状況です。
マネジメント体制
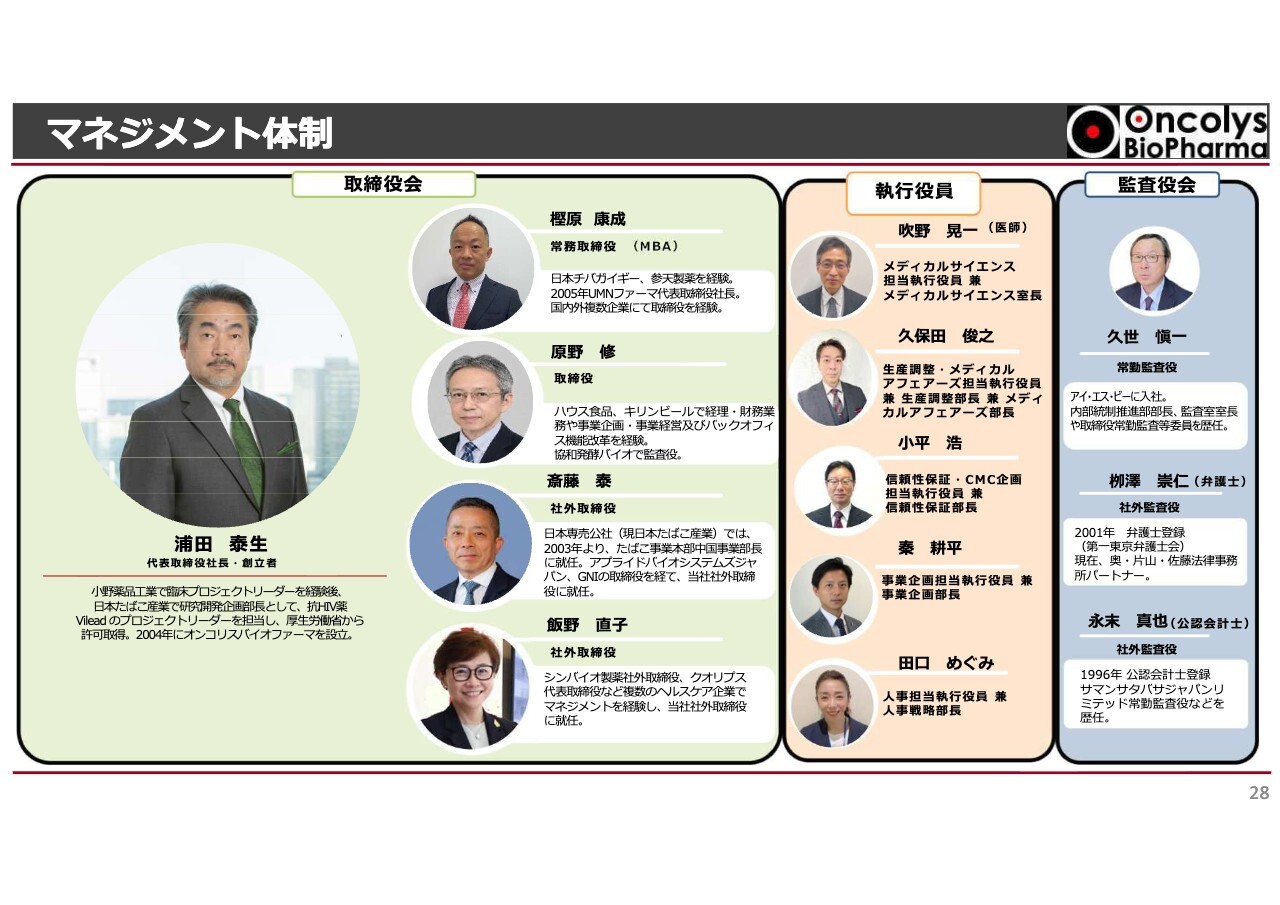
当社のマネジメント体制について、執行役員を中心とする各執行役員より、事業内容および目標について簡単に説明します。
吹野晃一(医師)

吹野晃一氏:メディカルサイエンス担当執行役員・CSO(チーフサイエンティフィックオフィサー)を務めている吹野です。
私は医師として臨床や研究に携わった経験を活かし、承認取得に向けた研究開発計画の立案、開発試験の実施、そして得られたデータを基に有効性や安全性を規制当局と議論する責任を担っています。
2026年は、「テロメライシン」で新たな効能を獲得するための効能拡大試験を実施するとともに、次世代ウイルス「OBP-702」を初めて人に投与する臨床試験を開始します。
テロメライシンは食道がん領域でどのように使われるか?
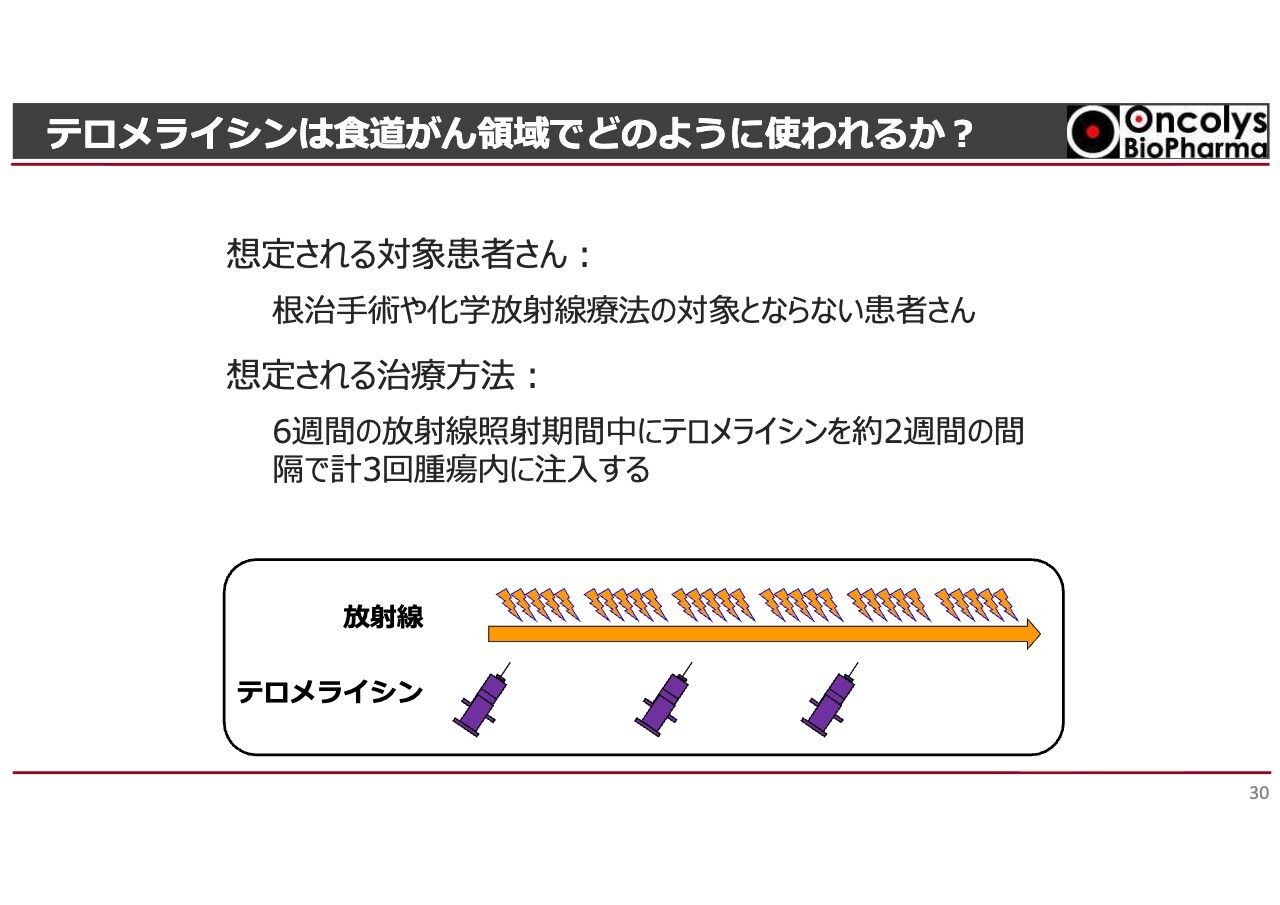
「テロメライシン」の食道がんに対する審査が現在佳境を迎えています。本日もお話ししたとおり、対象となるのは標準治療を受けられず、臓器機能や体力が低下した患者さまです。その患者さまに対して、放射線を併用しながら「テロメライシン」を3回投与するという使い方になると想定しています。
食道がん領域の満たされないニーズ
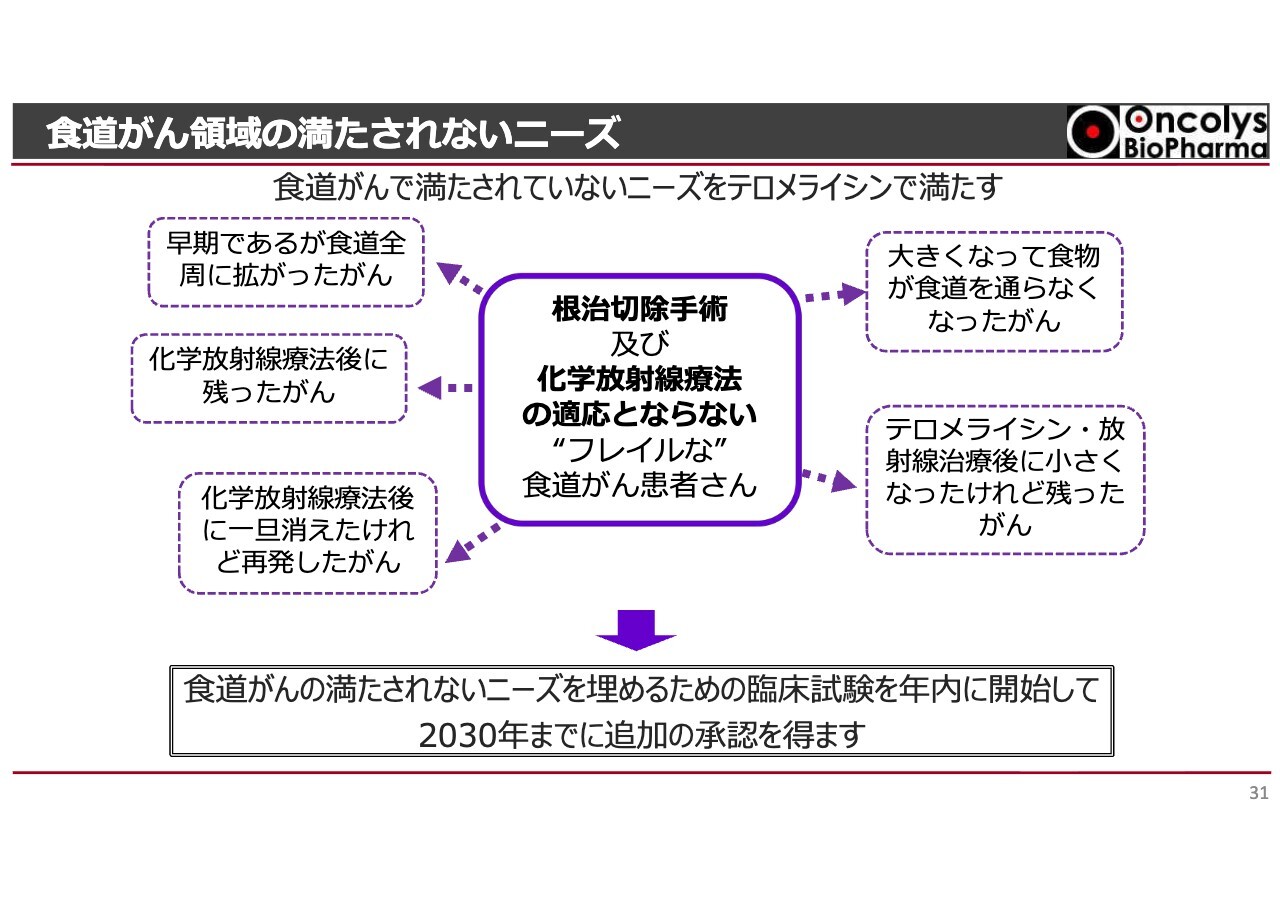
食道がん領域には依然として満たされていない医療ニーズが存在します。例えば、標準治療である化学放射線療法を受けた患者さまでも、3割から4割程度の方はがんが消えなかったり、再発してしまう場合があります。そのような患者さまに対する治療はまだ確立されていません。
当社は、食道がん領域における残されたニーズを一つひとつ検討し、どのニーズから取り組むべきか優先順位をつけて、新しい臨床試験を年内に開始します。
最大の腫瘍縮小効果
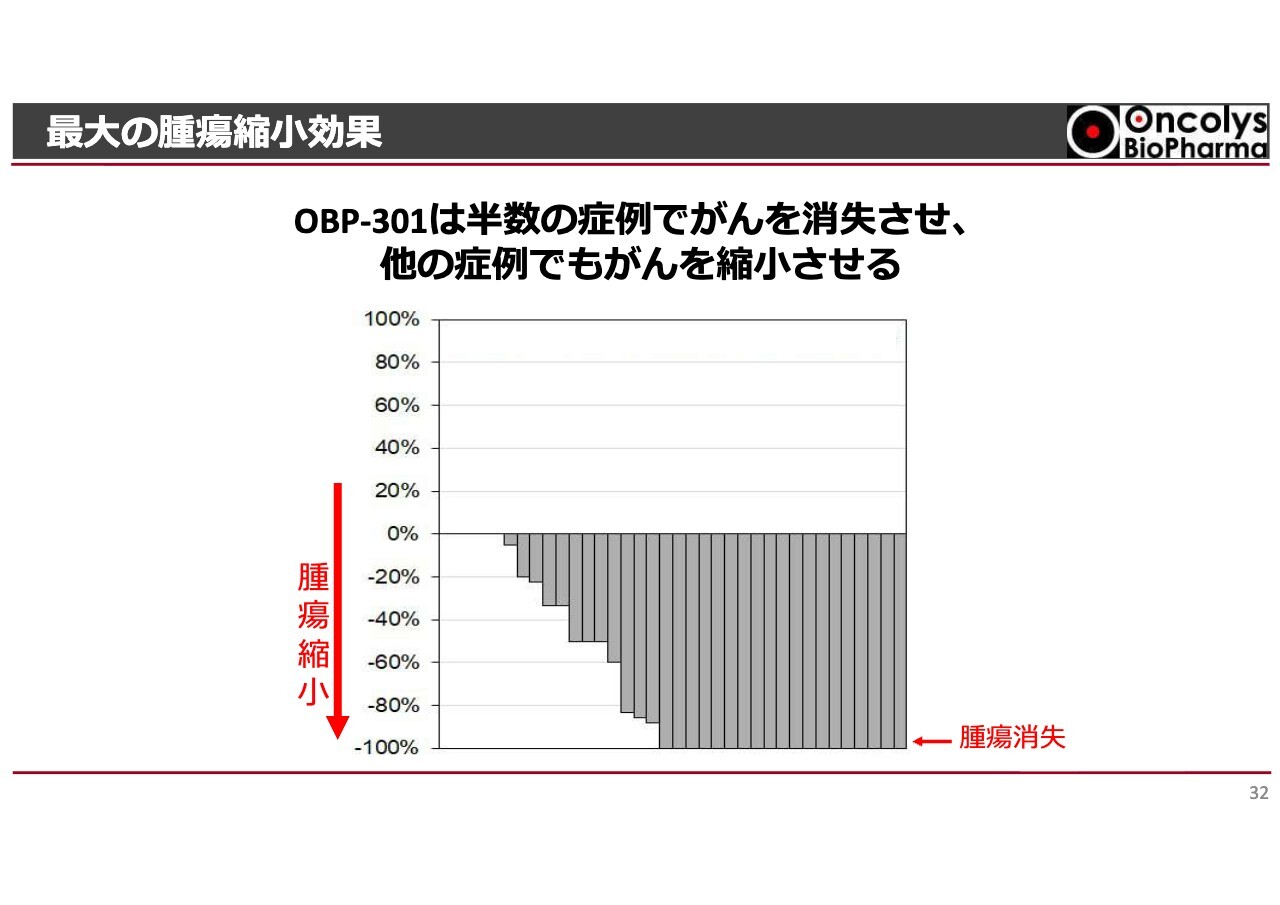
投与の結果、がんにどのような効果が現れるかを評価する方法の1つとして、治療開始前の腫瘍の大きさと、治療後に最も効果が現れた時点の腫瘍の大きさを比較する手法があります。
「テロメライシン」の場合、患者さまの半数で腫瘍のサイズが縮小する方向に動いており、そのうち半数は腫瘍が完全に消失する、すなわち縮小率がマイナス100パーセントに達するところまで振り切れるという結果が示されました。スライドのグラフから、「テロメライシン」の局所効果について非常によくおわかりいただけるかと思います。
OBP101JP試験のがん関連生存率
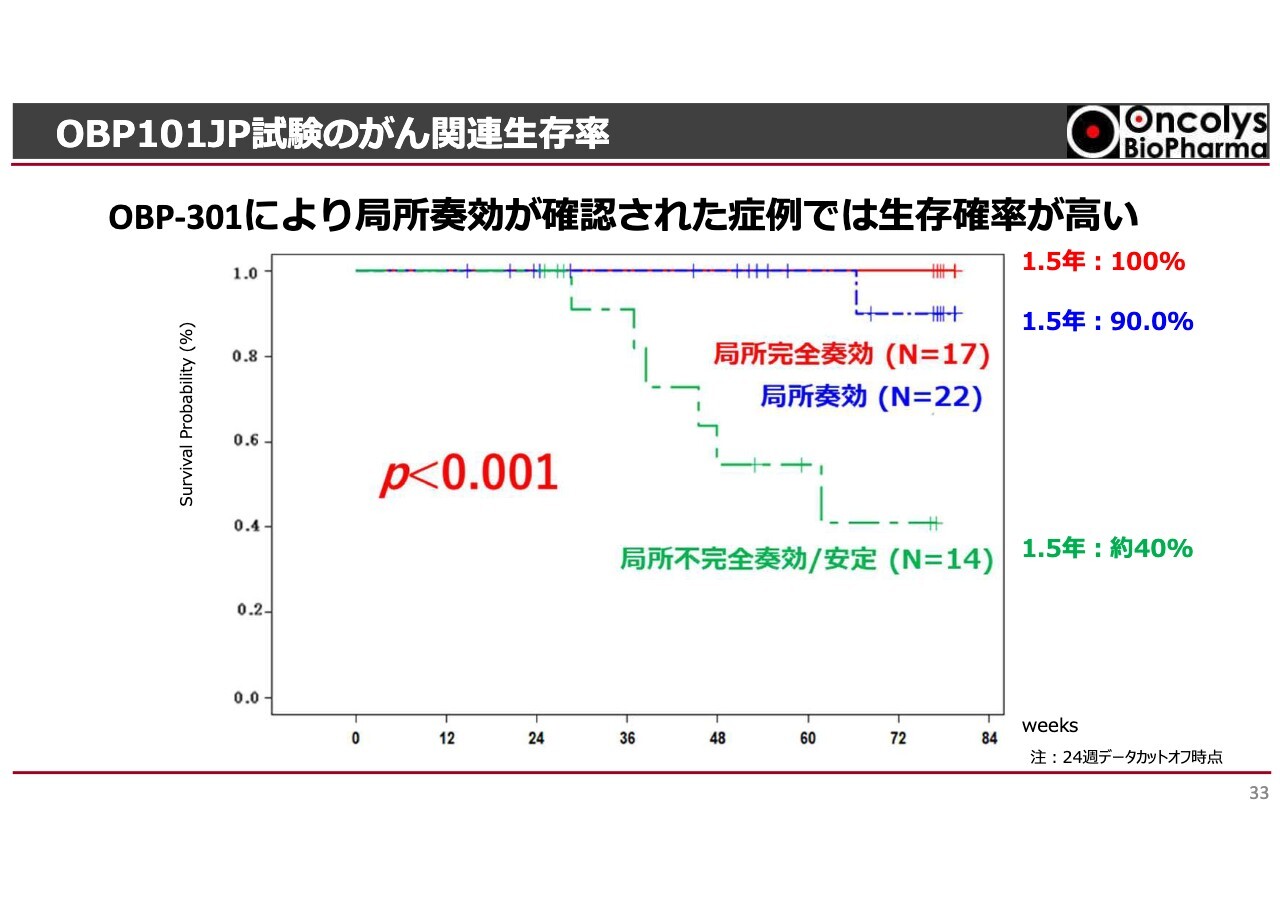
抗がん剤の分野では、局所以外にどの程度生存期間を延ばせるか、生存する患者数を増やせるかという点も注目されています。
「テロメライシン」で局所に十分な効果が得られた患者さまについては、この1年半の臨床試験期間中に食道がんが進行して亡くなった患者さまがほとんどいなかったことが確認されました。局所治療薬ではありますが、生存期間の延長にも貢献していることが確認されています。
食道がん以外で満たされないニーズを埋めて行く
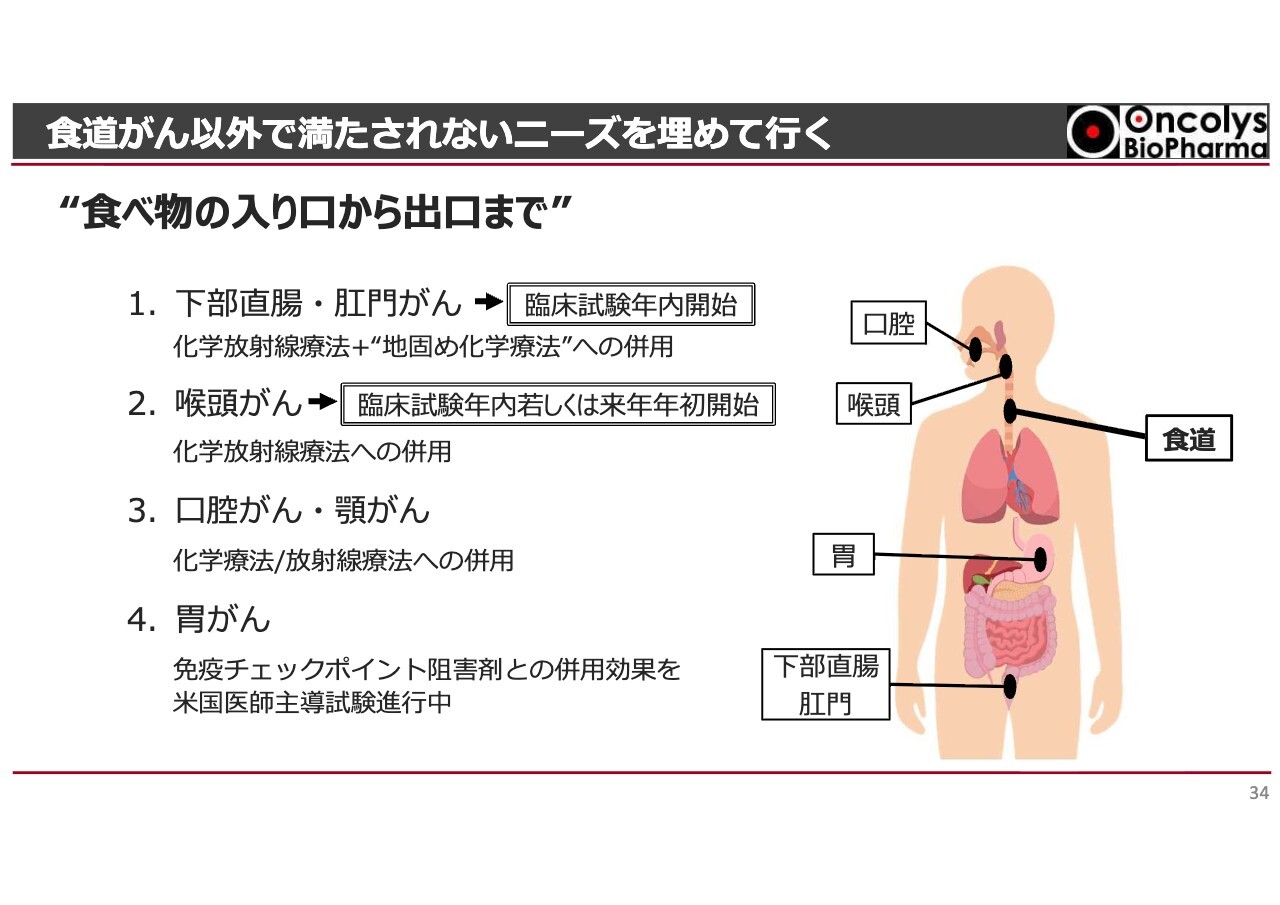
食道がん以外に目を向けてみると、例えば食べ物の出口に該当する肛門の部分に腫瘍ができた場合、最近の臨床現場では、いきなり手術をするのではなく、まず化学放射線療法を実施します。そして、そこで効果が得られた患者さまには、その後「地固め」と呼ばれる化学療法を追加することで、人工肛門を作る手術を回避しようという方向性が広がっています。
当社もその流れに沿い、化学放射線療法に「テロメライシン」を併用することでその効果を高め、人工肛門を必要とする患者さまを減らすことを目指しています。すでに大腸がん診療専門医をはじめとする先生方とディスカッションを行い、計画を練っています。この臨床試験を年内に開始する予定です。
もう1つ重要な機能として、声を出すという機能があります。声を出す場所は喉の奥にある喉頭という部分ですが、この部分を手術で大きく切除すると、声が完全に失われることになります。小さく切除しようとしても、術後に引きつれが起きるなどして声がうまく出せなくなることがあります。
このような患者さまに対して、「テロメライシン」を用いて声を守る、あるいは喉頭がんの患者さまに「テロメライシン」を用いて声を守るという計画について、耳鼻咽喉科の先生方と議論を始めています。この臨床試験についても、年内もしくは来年年初の開始を目指し、準備を進めています。
p53遺伝子をもつ次世代腫瘍溶解ウイルス OBP-702
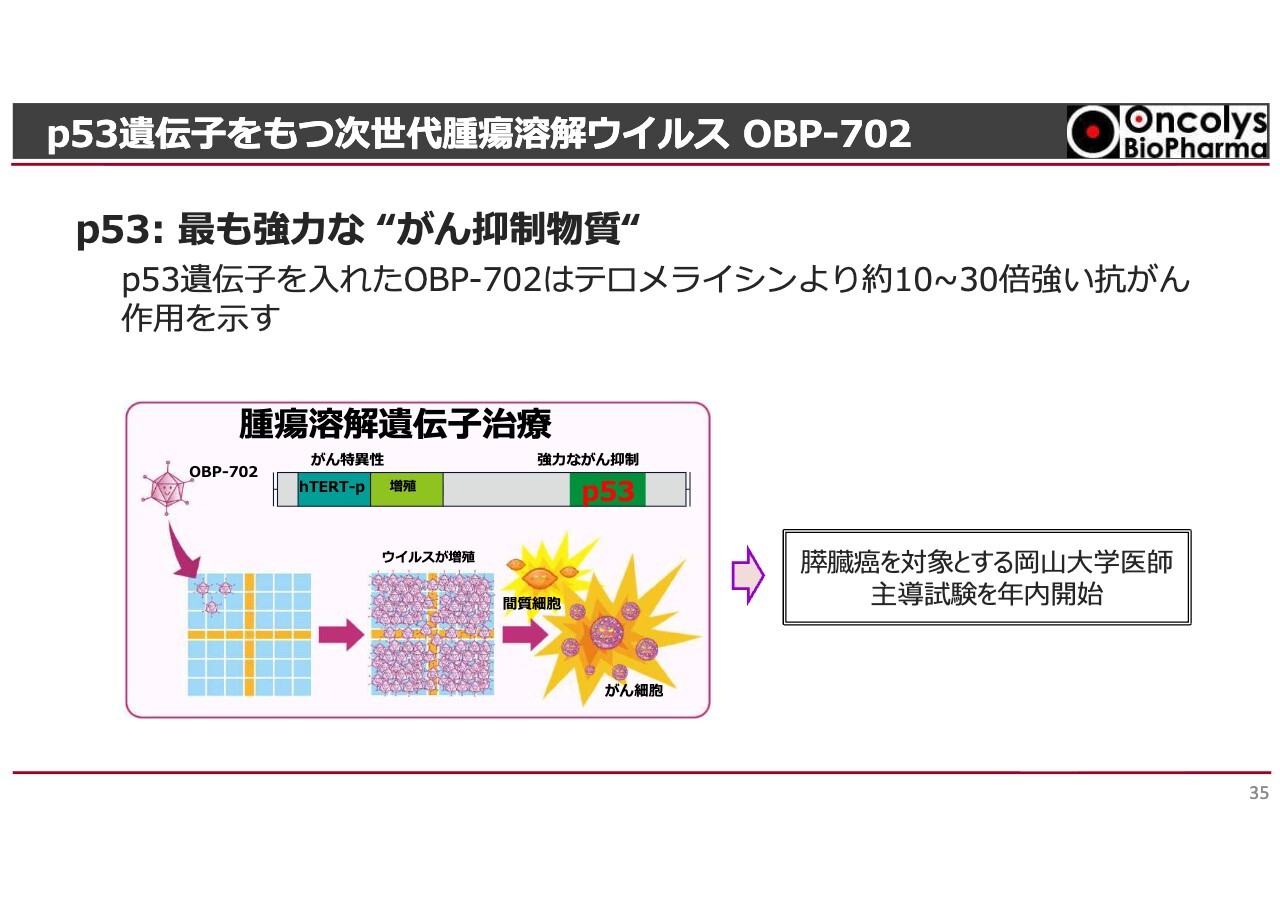
最後に、次世代のウイルスについてお話しします。私たちの体内では、正常な細胞ががん細胞へと変化することを抑制する物質が働いています。それらの物質をがん抑制物質と呼んでいますが、その中でもp53は最も強力な作用を持っています。
p53遺伝子をもつ次世代腫瘍溶解ウイルス OBP-702
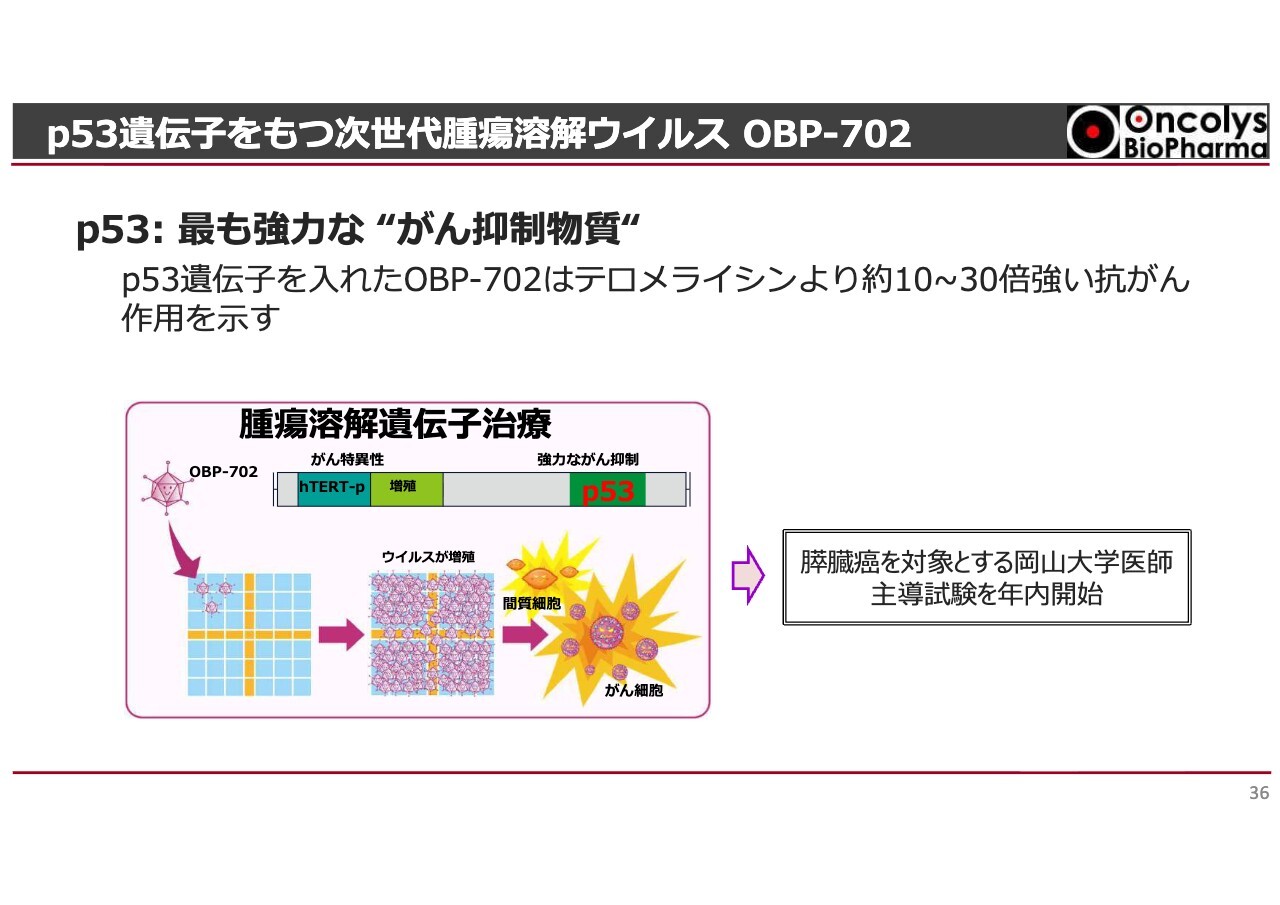
次世代腫瘍溶解ウイルス「OBP-702」は、p53の遺伝子を導入することで「テロメライシン」よりも強い抗がん作用を発揮することが期待されています。そして、岡山大学の医師主導試験として、初めて人への投与を行う臨床試験を年内に開始する予定です。
「2026年にご期待頂きたい事項」
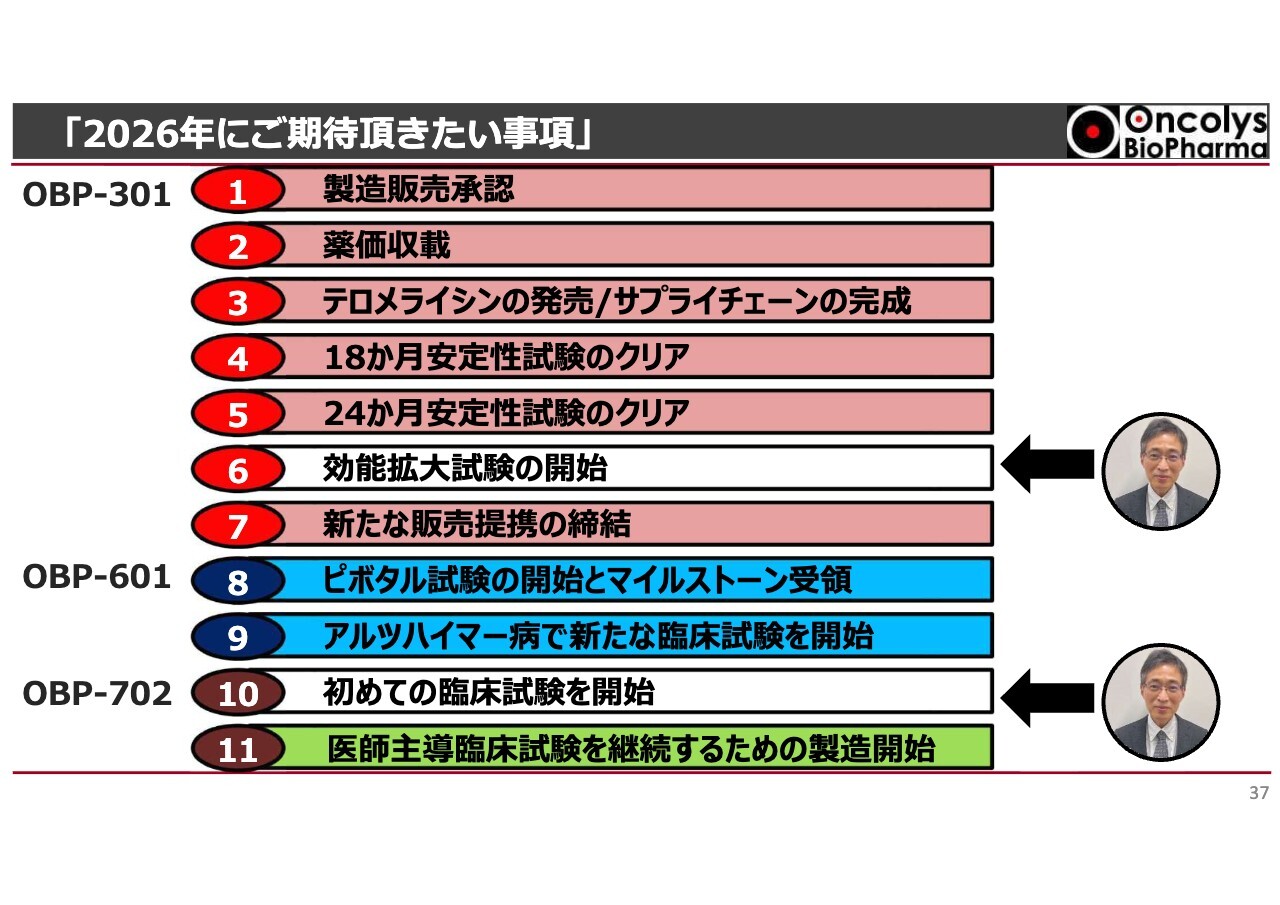
2026年にご期待いただきたい臨床開発に関する項目として、「テロメライシン」の効能拡大試験の開始、次世代ウイルス「OBP-702」の初めての臨床試験開始をお約束し、私からの説明を終えたいと思います。ありがとうございました。
久保田俊之

久保田俊之氏:生産調整・メディカルアフェアーズを担当しています久保田です。よろしくお願いします。
私は生産調整とメディカルアフェアーズを担当しています。具体的には、当社が開発・製造した「テロメライシン」を患者さまに安定的に届けるためのプロセスを構築し、管理する役割を担っています。
メディカルアフェアーズのパートについては、患者さまへ届いた薬を使用して治療を行う際に、「実際にその治療が正しく行われているか?」「さらに良い治療はどのようなものか?」について医療現場の先生方と共に考え、医療環境を整える仕事をしています。
サプライチェーンに関わる整備状況
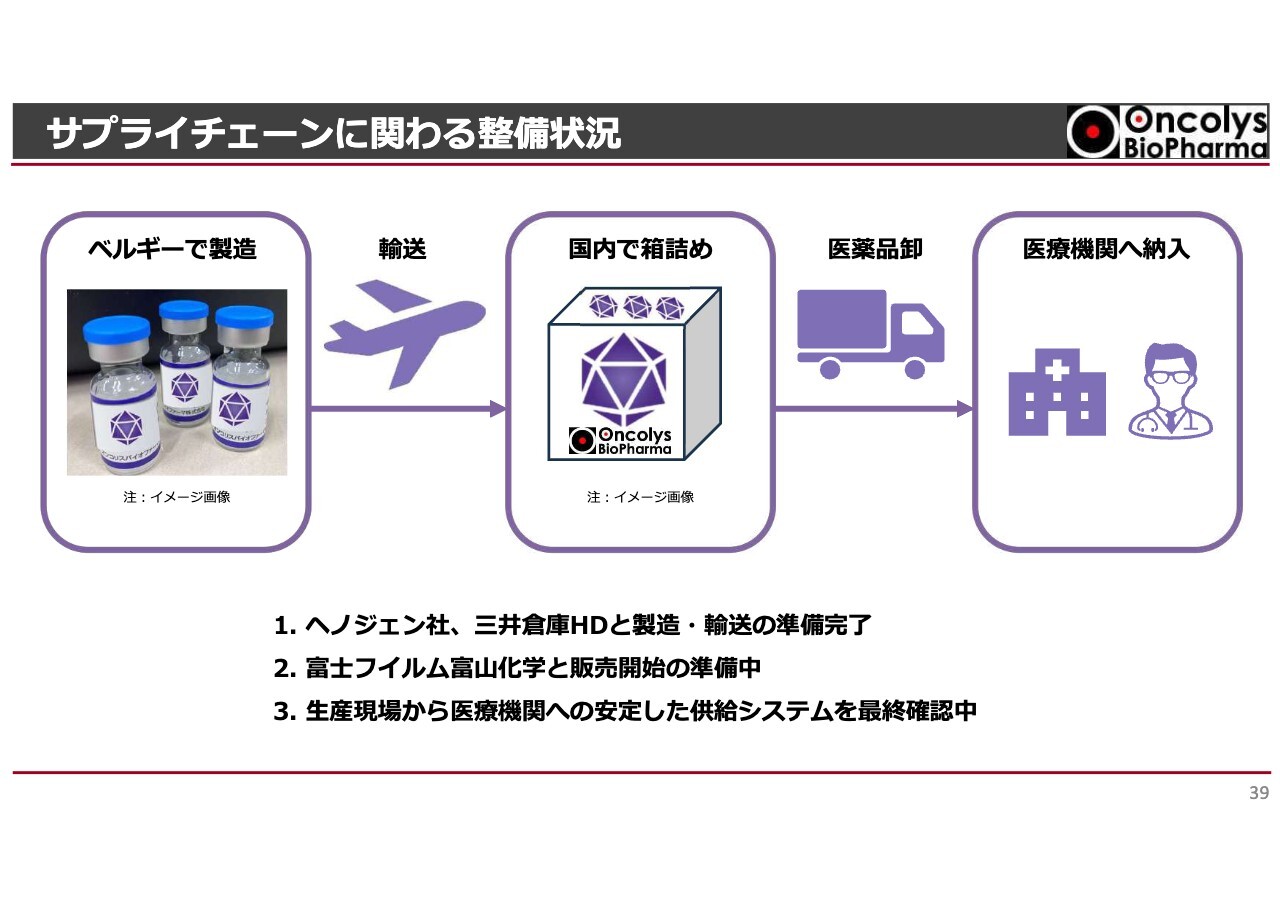
まず、サプライチェーンに関する整備状況についてお話しします。冒頭に浦田社長からもお話がありましたが、「テロメライシン」はベルギーのヘノジェン社で製造され、マイナス80度で保管されています。「テロメライシン」はマイナス80度を保った状態で日本に輸送し、日本国内で箱詰めをして医療現場に届けるというプロセスを経ます。
この間、マイナス80度を維持したまま輸送することは非常に困難であり、ここ数年間、何度もテストを繰り返してきました。現在では、ヘノジェン社と三井倉庫ホールディングスの協力により、マイナス80度を安定して維持した状態で日本に輸送し、箱詰めまで完了させる体制を整えることができました。したがって、箱詰めまでの準備はすでに完了しています。
実際に箱詰めされたものが医療現場に届けられるプロセスについては、富士フイルム富山化学と、その医薬品卸業者の方々とともに構築を進めているところです。現在、プロセスの最終段階にあり、間もなくすべてが完了する予定です。
これにより、サプライチェーンはほぼ完成となります。あとは承認後の発売を待つだけという状態に持っていけるよう、今年は全力を尽くしていきたいと考えています。
テロメライシンの安定供給

これまでご報告してきたとおり、ウイルスの性質上、製品がやや濁ったように見える場合がありました。しかし、濁りのない製品の製造に成功し、さらに18ヶ月の安定性を確認していることについては、すでにご報告のとおりです。
今後は有効期限を24ヶ月、36ヶ月と延ばし、「何本製造して、かつどれだけ売れてきたときには、その在庫がしっかりと保った状態で患者さまに届けられるように管理をしていこう」といった役割を、門番のようにしっかりと管理し、安定供給を達成したいと考えています。
テロメライシンをより多くの患者さまへ届けるために
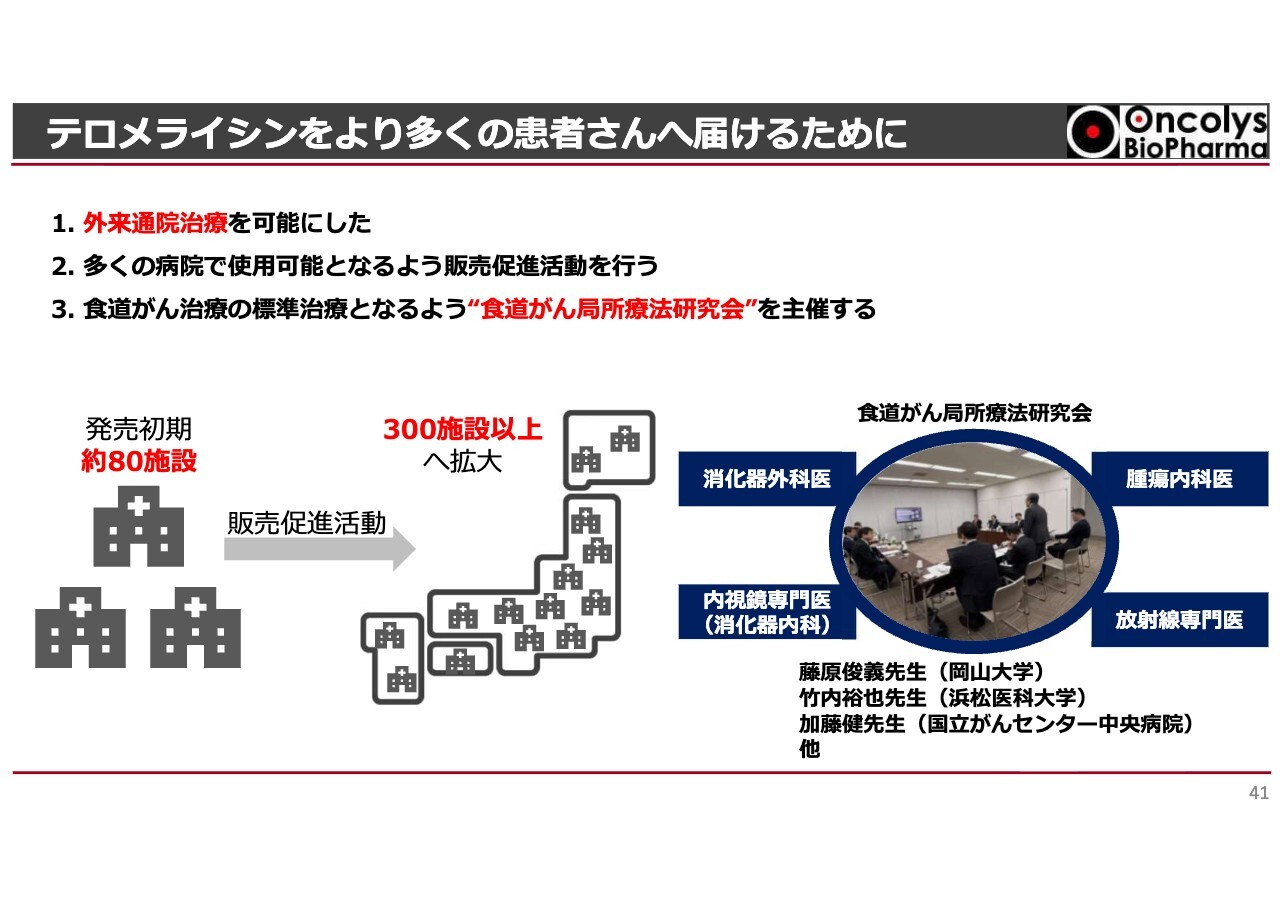
先ほど浦田社長よりご説明のとおり、メディカルアフェアーズとして「テロメライシン」が実際に使われるようになったことで、これまでは治験で必須だった入院が不要となり、外来で使用できるようになりました。これは大きな成果です。外来通院が可能になることによって、より多くの病院で実際に治療が行えるようになると考えています。
ただし、発売当初からすべての病院で使用できるわけではなく、その準備には時間がかかるものと認識しています。まずは、食道がんの治療を中心に行っている拠点病院80施設に対し、富士フイルム富山化学と協力してしっかり導入を進めていきたいと考えています。
その後、ほぼ日本全体の食道がん患者さまをカバーできる治療を提供できるよう、300施設以上まで対象を拡大し、病院への導入を進めていきます。
こうした活動を通じて実際の投与経験が蓄積されることで、その情報を「食道がん局所療法研究会」で議論し、さらに発展させていきたいと考えています。
藤原教授、竹内先生、加藤先生をはじめとする食道がんのエキスパートの先生をはじめ、内視鏡専門医や腫瘍内科医、放射線専門医と共に議論を重ねながら、「より良い治療とはどのようなものか?」「『テロメライシン』はどのような患者さまに投与されて、どのような結果をもたらすのか?」についての研究を市販後も進めていきたいと考えています。
「2026年にご期待頂きたい事項」
2026年の「テロメライシン」の発売に向けて、しっかりと承認を取得し、その後に患者さまへ届けられるよう、準備を進めていきます。達成に向けて最善を尽くしますので、どうぞよろしくお願いします。ありがとうございました。
小平浩

小平浩氏:総括製造販売責任者として信頼性保証・製造品質管理を行い、CMC企画部を担当している小平です。
テロメライシンの品質管理と安全管理
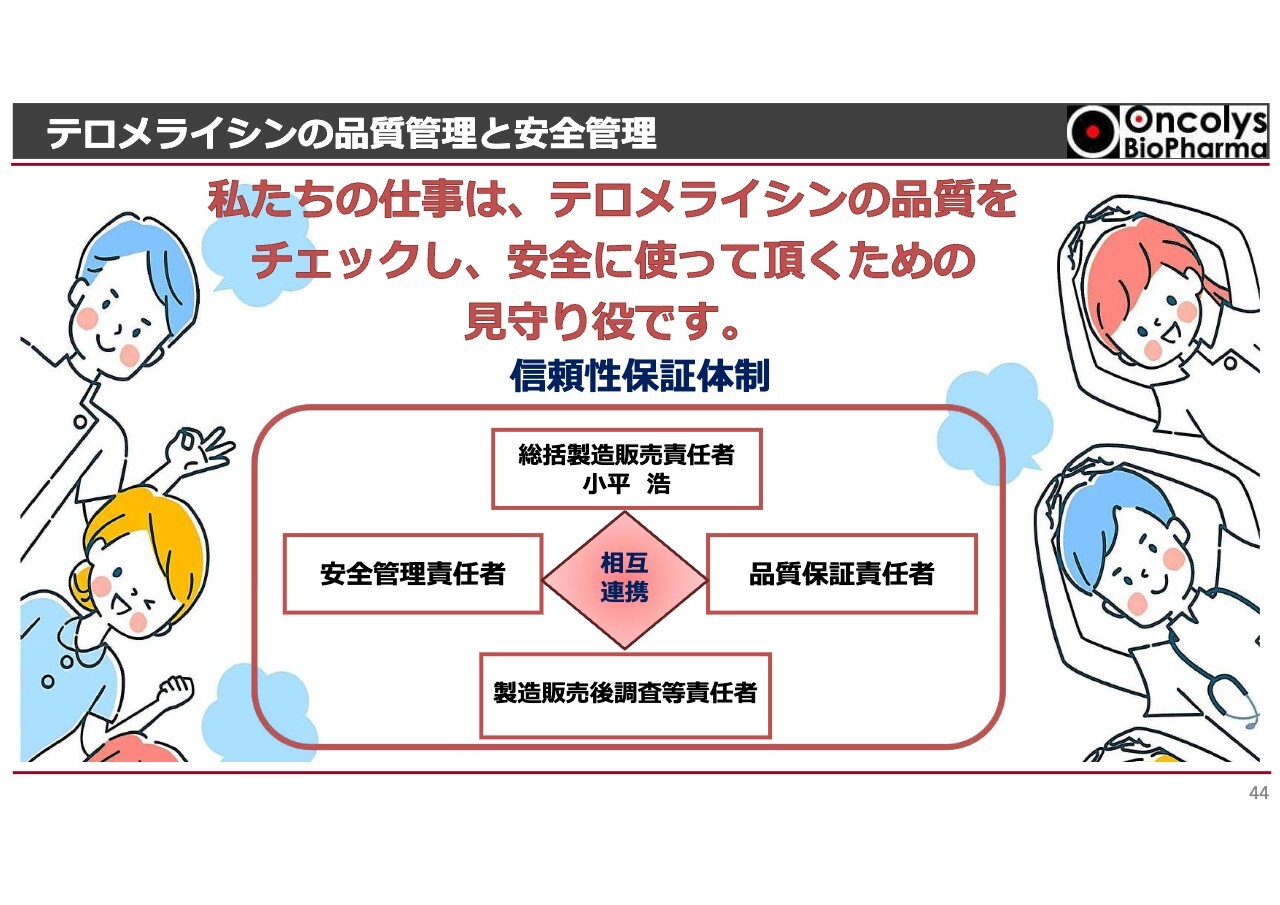
信頼性保証では、安全管理責任者、品質保証責任者、製造販売後調査等責任者と連携し、「テロメライシン」の品質および安全管理に取り組んでいます。また、CMC企画では「テロメライシン」および「OBP-702」の製造並びに品質管理に関する業務を担当しています。
当社は2025年4月に製造販売業許可を取得しました。製造販売業許可の構成については、安全管理部門と品質保証部門の2部門で構成されていますが、当社ではこれに再生医療等製品の製造販売後調査部門を加えた3部門体制で「テロメライシン」の品質および安全を担当しています。
品質保証業務としては、工場から提供される製造記録や試験検査記録を評価し、最終的に問題がなければ出荷判定を行います。また、出荷後の製品に苦情やクレームがあった場合には、それに対応していきます。
安全管理部門においては、病院や患者さまから寄せられる副作用情報の評価を行い、検討が必要な副作用情報に関しては専門家の意見を聞き、その対策を立てたうえで、必要に応じて医療機関に注意喚起を行います。
製造販売後調査部門では、通常の承認後に厚生労働省から安全性のさらなる検討の指示が出されます。その調査を計画し、実施していく予定です。
当社は安全性および品質に関して、「テロメライシン」を適切に見守る役割を担うべく、この3部門の体制で進めていきたいと考えています。
扱いやすい製剤への改良

ここからは、製造に関する当社の取り組みについてご説明します。「テロメライシン」はマイナス80℃で保管されています。研究分野でも、一般的にウイルスはマイナス80℃で保管されることが一般的であり、マイナス80℃という温度は特別な保管温度ではありません。ただし、輸送や病院での取り扱いを考えると、溶けている4℃の製剤があると非常に便利です。
当社はこれまで、マイナス20度での保管温度について予備的な安定試験を実施し、「テロメライシン」においてはマイナス80度と変わらないデータを得ています。しかし、4度での安定にはまだ至っていません。
今後は、安定性のある製剤の開発を目指し、安定化剤の検討などを進めていきたいと考えています。
製造体制の編成(製造所の追加・OBP-702の製造)
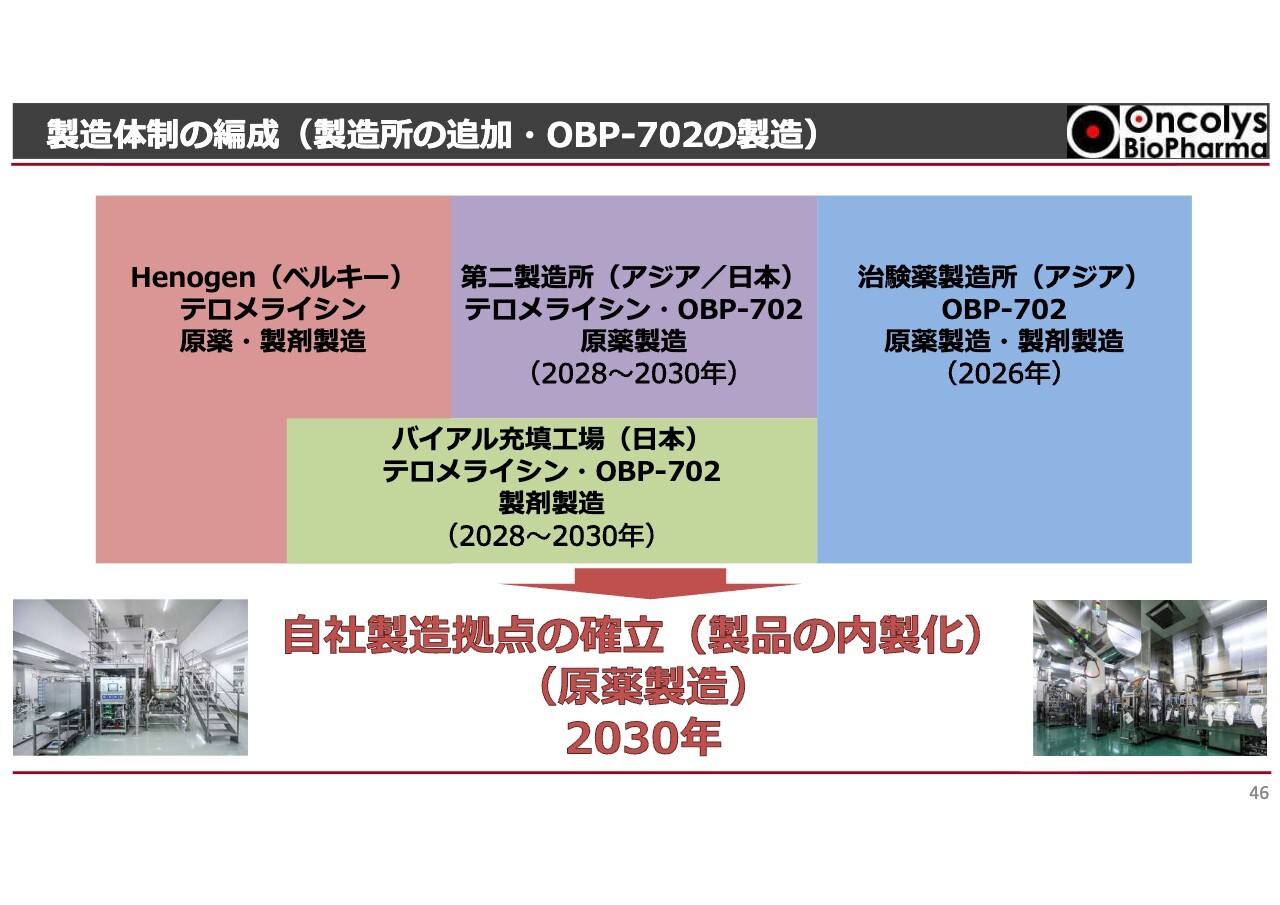
製造体制の編成についてご説明します。「テロメライシン」はヘノジェン社のみで製造されています。今後の販売拡大や海外展開を見据えると、安定供給に対する不安が残るため、第2の工場を準備したいと考えています。具体的には、製剤の工場と原薬の工場をそれぞれ1つずつ用意し、「テロメライシン」だけでなく「OBP-702」にも適用できるようにしたいと考えています。
今年は「次世代テロメライシンOBP-702」の臨床試験が始まる年です。当社は「OBP-702」の製造をアジア圏で行い、岡山大学が実施する医師主導型臨床試験に提供していきたいと考えています。
最後に、第二製造所の追加や製品の改良技術を蓄積し、最終的には技術者を育成していきます。そして、2030年までに製造拠点を設け、その後の製品内製化を進めていきたいと考えています。
「2026年にご期待頂きたい事項」
最後となりますが、「テロメライシン」の24ヶ月安定性試験のクリアおよび「OBP-702」医師主導型臨床試験を継続するための製造開始についてお約束します。ありがとうございました。
樫原康成

樫原康成氏:事業開発兼リスク管理担当の樫原です。私からは、今後どのように海外展開を進めていくかをご説明します。
海外展開による成長機会の拡大

2019年に先駆け指定をいただき、日本での発売を目指して活動してきました。この点についてはご説明のとおりですが、その結果として、今年から発売できる体制が整ってきていると考えています。
この後、日本で発売を進めることに加え、海外からも資金を獲得する道筋を構築することが、当社の今後の成長に非常に重要であると考えています。
日本での承認を基に海外での承認を取得し、販売提携を進めることで、海外からの資金を獲得できる基盤を整えていきたいと考えています。具体的には、アジアに注目していきたいと考えています。
どの国・地域を優先するべきか?

スライドの図はWHO(世界保健機関)から公表されている患者数のデータです。ご覧いただくとおわかりのように、食道がんの患者はアジアに非常に多く、世界全体の70パーセント以上がアジアに集中している疾患です。このような状況から、アジアに集中して提携を進めることは極めて合理的であると考えています。
日本承認を起点とした海外展開戦略(1)

具体的にどのように進めていくかについてご説明します。まず、患者数が多いアジア地域です。2024年12月に台湾のMedigen社と契約を結んでおり、台湾においてはMedigen社が中心となって商業化を進めていく予定です。日本の承認申請データを活用し、できる限り早く承認を取得する方法を現在検討しています。
また、韓国、シンガポール、香港、タイといった国々に対しては、どのように承認を取得し、販売を進められるかを検討しています。これらの国々を対象とする製薬会社と協議し、販売提携の交渉も進めています。
先ほどご覧いただいた図では、アジアの中でも中国が半分以上を占めており、中国は重要な市場ではないかとのご意見もあるかと思います。一方で、当社のこれまでの経験から、中国で発売を進めるには新たに追加の臨床試験が必要になることや、中国国内で製造する必要があることなど、コスト負担が非常に大きくなる可能性がある点を懸念しています。そのため、中国以外のアジア諸国を優先的に事業展開していきたいと考えています。
日本承認を起点とした海外展開戦略(2)

先ほどの患者数でもお伝えしたように、EUや英国にも非常に多くの患者さまが存在します。一部の国では、日本で当社が承認を目指している放射線と「テロメライシン」の併用が想像できる地域もあります。
英国については、英国独自の薬事制度があり、日本を含む海外のデータを活用して承認を取得できる仕組みがあります。この制度を活用し、イギリスでの早期承認を目指して取り組んでいきます。また、現地のどの製薬会社と連携するかについても協議を進めていく方針です。
冒頭に浦田社長から米国での臨床試験で良い結果が出ているとご報告がありましたが、米国で開発を進めるためには非常に大規模な臨床試験を実施する必要があります。患者数は日本と同程度の規模である場合もありますが、コスト対将来の収益を考慮し、アジアおよびEU、英国を優先的に進めていきたいと考えています。
「2026年にご期待頂きたい事項」
最後に、すでに2月の決算説明会の後にもご報告しましたが、新たな提携を進めることで、今後の収益獲得に貢献していきたいと考えています。また、年内に1社以上と契約を締結することを約束したいと考えています。引き続きご支援を賜りますよう、よろしくお願いします。
秦耕平

秦耕平氏(以下、秦):事業企画担当執行役員の秦耕平です。事業企画部では株主のみなさまをはじめとした投資家のみなさまとのIR活動や、マスコミ等のPR活動を行っています。
また、株式の発行による資金調達や、今年2月に発表したみずほ銀行からの借り入れなど、銀行からの借り入れ業務を行っています。その他、事業会社とのアライアンス活動も進めています。
2025年1月以降の株価推移
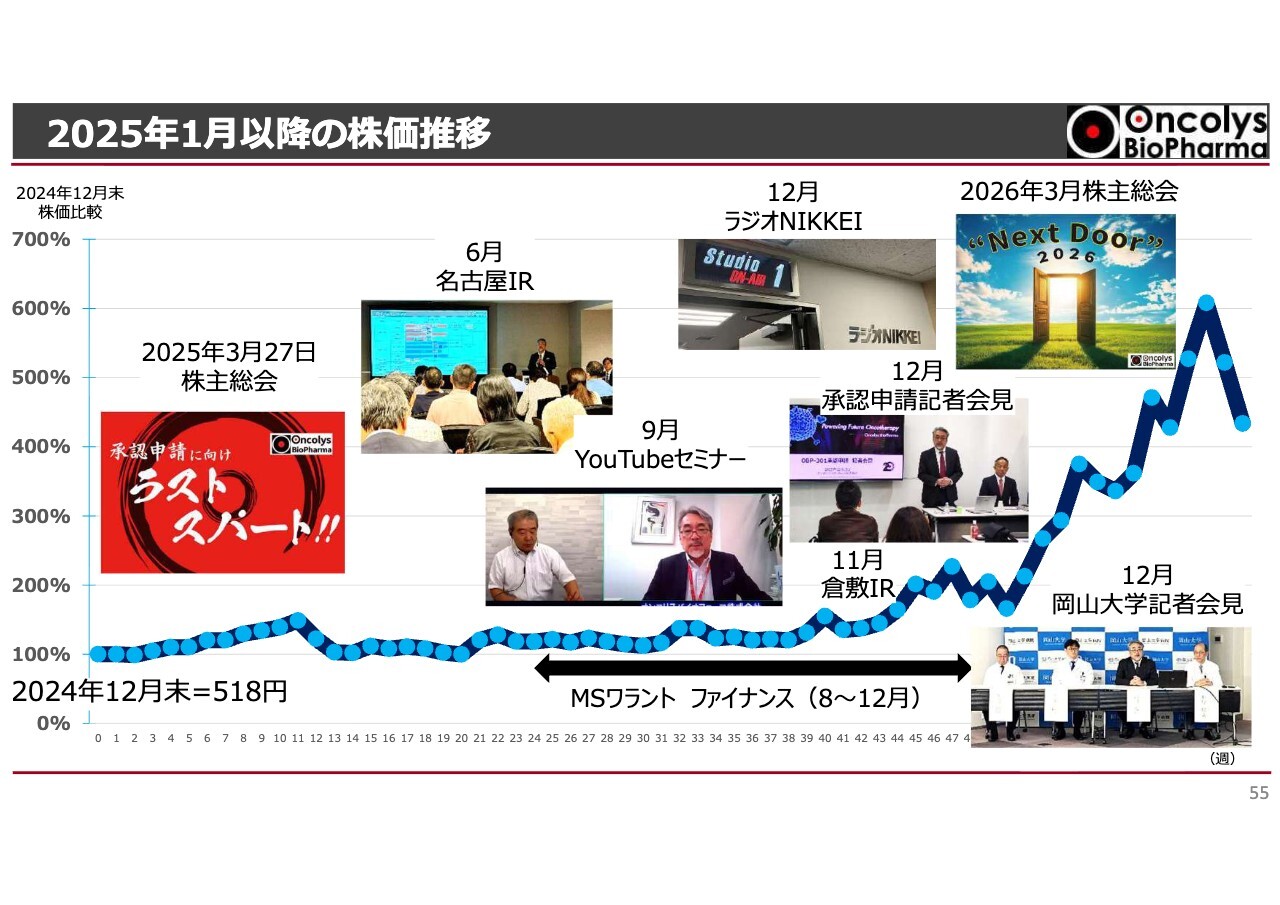
2025年1月以降の株価の推移についてです。1年前、この場で「テロメライシン」の承認申請に向けた活動を積極的に市場へ報告することをみなさまに約束しました。
2025年1月以降、株価が一本調子で右肩上がりに推移したわけではありません。途中、やむを得ずMSワラントによるファイナンスを実施した時期もあり、株価が横ばいの時期もありましたが、昨年12月に承認申請を行った後、株価は堅調に推移しています。
最近は、機関投資家やアナリストとの面談で「御社は『テロメライシン』の許可を取ることだけを、目的にしていないですね」という評価を受けることがあります。
浦田社長や執行役員がご説明してきたように、承認後に「テロメライシン」を普及させ、効能を拡大し、当局への報告をきちんと行う、といった未来に向けた準備をしっかりと進めていることが、直近で時価総額が拡大している要因の1つであると考えています。
新しいTOPIXの採用基準
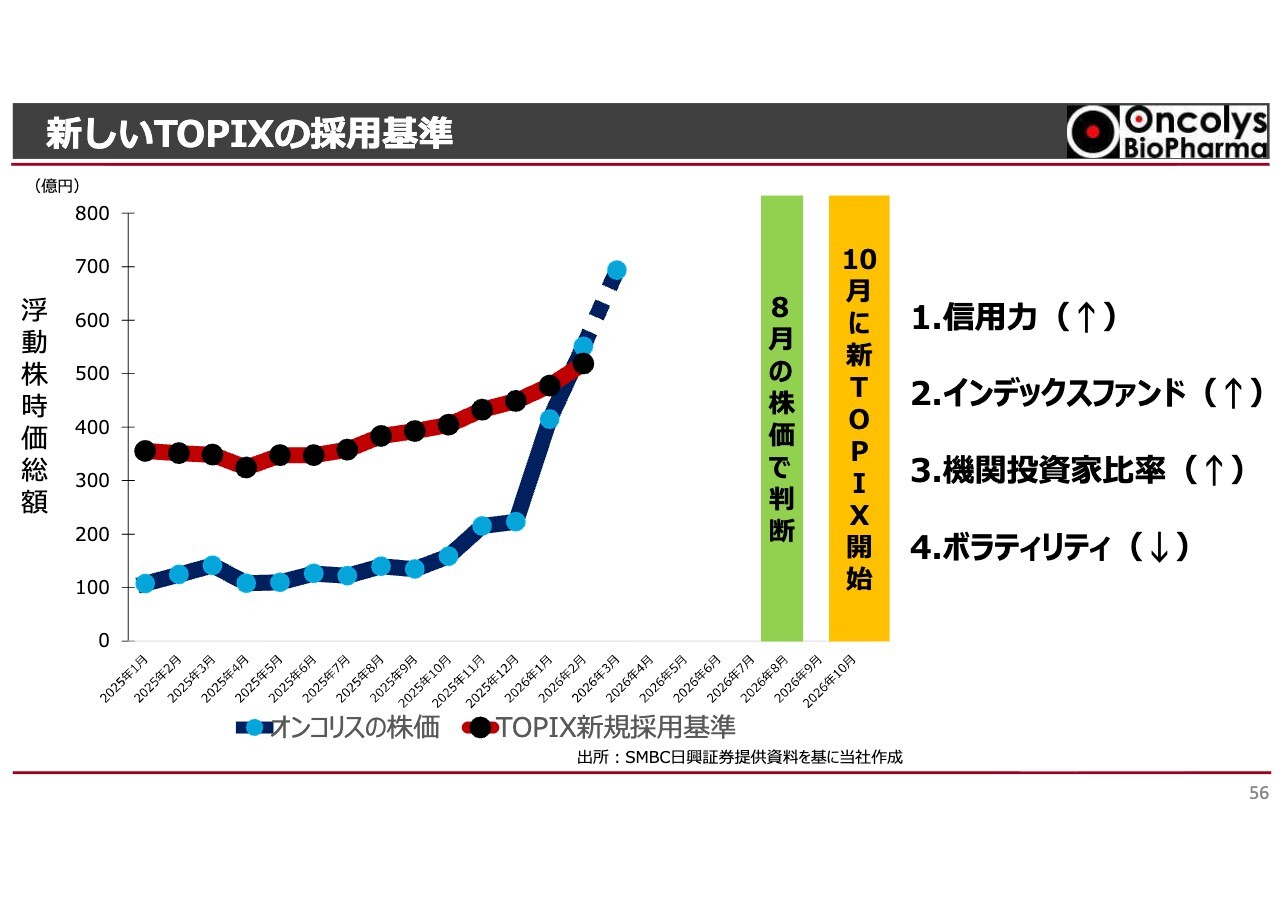
先ほどの株主総会でも議案の一部で触れましたが、TOPIXの採用に関する見通しについて報告します。TOPIXは東証株価指数のことで、東京証券取引所の市場改革の一環として、今年10月から新たな制度に切り替わります。
採否に関しては今年8月の株価水準で判断されますが、新規採用基準を今年2月の時点で上回っており、3月時点でも上回ると見込んでいます。
このまま推移してTOPIXに採用されると、当社のレピュテーションが向上するとともに、インデックスファンドなどの投資家からの機械的な株式の買い付けにより、機関投資家の比率が向上し、ボラティリティの低下といった効果が期待されます。
ただし、TOPIX採用に関しては当社の努力だけで達成できるものではありません。相対的な浮動株時価総額の順位が影響するため、他社との比較の中で決まる要素も含まれます。それでも、しっかりとチャレンジしていきたいと考えています。
財務面の新たな展開

当社は今年、「テロメライシン」の集大成として創薬型ベンチャーから製薬型へ移行する中で、財務面でも新たな展開を進める方針です。IR活動やメディアリレーションズ活動を引き続き拡大し、認知度を一層高めていきます。
また、銀行からの借り入れを通じて、「テロメライシン」の製造・出荷から資金回収までの一連のサイクルを資金面でしっかりとサポートする計画を進めていきます。
事業パートナーとのアライアンスを通じて、事業の進展を図っていきたいと考えています。今年の2月の決算説明会でもお伝えしたとおり、今年はMSワラントなどのファイナンスを実施せず、事業を進展させるための資金をしっかりと確保していく方針です。
以上で説明を終わります。
田口めぐみ

田口めぐみ氏:人事担当執行役員の田口です。私は人事戦略部を担当しています。
今後の人事戦略『採用と人財育成』

事業計画に伴う人事戦略についてお話しします。採用と人材育成の観点から、2つのポイントについてお話しします。
昨今、バイオ業界や再生医療業界を含む他業種においても、非常に激しい人材獲得競争が繰り広げられています。このような状況の中で、当社としては優秀な人材を獲得すること、そしてご入社いただいた人材が社内で自己成長を実感できるような育成・成長環境を提供することが重要であると考えています。
具体的に、採用と人材育成についてお話しします。採用については、優秀な人材の大幅な増員を計画しています。先ほどの吹野執行役員のご説明にもあったように、パイプラインの進行や適応拡大に対応するため、現在10名以下の体制で運営している開発人材を15名程度に増員する考えです。
また、小平執行役員よりご説明があったバイオ製剤製造に関しても、この分野のスキルを有した人材を15名体制に拡充していく予定です。
さらに、過去の決算説明会でもお伝えしてきたとおり、当社はこれまで少数精鋭で優秀な人材を採用してきました。先ほどの株主総会でも、当社の少数精鋭の体制に高い評価をいただきました。しかしながら、現在在籍している社員の質を維持しつつ、これからはより多くの人材を採用していきたいと考えています。
そのような採用活動の中で、候補者の方々からいただいた情報をもとに、当社の強みを3点にまとめています。まず1点目は、パイプラインの魅力です。先ほどからお話ししている腫瘍溶解ウイルスなどが非常に魅力的だと感じていただいています。
また、「がんを切らずに治す」という社会的意義の高い事業に共感を得ています。さらに、アデノウイルスを使ってがんを治療するという非常に新しいモダリティに対して革新的に挑んでいるという点、こうしたベンチャー要素を持ちながら、ライセンスビジネスから製薬企業へと進化していく成長性と安定性があるといった点にも深い関心をお寄せいただいています。
選考の最終段階では、浦田社長にも参加していただいており、面接の後半は社長に対するウイルスや関連分野の質問が多くなる傾向があります。選考の場面では、サイエンス講義のようなかたちになることも多々見受けられますが、こうした浦田社長の創業以来の一貫したリーダーシップやウイルス創薬に関するユニークな経験が、当社の大きな魅力の1つとなっています。
今後は、エージェントだけでなく、大学の研究室などにもアプローチを行い、人材獲得を進めていきたいと考えています。
一方、人材育成については2つの重点項目を掲げています。まず、研究開発人材の高度化についてです。社内外には、臨床医や科学者といった方々がいますので、そのような方々に定期的に社内講演を実施していただきます。
これを通じて、医学と科学の両面から知見を深化させ、研究開発力の底上げを目指していきます。また、次世代リーダーの育成についてです。社内には専門性を持ったスキルを有する方が多く在籍していますが、さらにマネジメントスキルを兼ね備えた人材を計画的に育成し、組織マネジメント力の強化を進めていきたいと考えています。
このように、採用と人材育成の2軸で会社の事業推進を進めていきたいと考えています。
以上です。ありがとうございました。
浦田氏からのご挨拶
浦田:長時間にわたり事業説明会をご聴講いただき、ありがとうございました。2026年もご期待に応えるべく、私も最大限尽力していきたいと思います。
各界からエキスパートを選りすぐり、現在の執行役員体制を構築してきました。この執行役員のメンバーがさらに成長し、事業を盛り上げ、拡大していくことを大いに期待しています。また、私自身も引き続き実行に関与していきたいと考えています。
また、冒頭でご説明したとおり、私はこの会社を立ち上げて22年の間「テロメライシン」に取り組んできましたが、今年は集大成の年となります。
引き続き、みなさまからのご支援、またご指導・ご叱責を賜りますよう、よろしくお願いします。ご清聴ありがとうございました。
質疑応答:「テロメライシン」の効能拡大に必要な期間について
質問者: 適応拡大についてご質問します。がんの種類によって治験にかかる時間は異なるため、一概にはいえないと思いますが、例えば肛門がんや喉のがんの場合、治験の開始から適応拡大の申請へ至るまでに、どの程度の時間を要するとお考えでしょうか?
浦田:大前提として、「テロメライシン」の食道がんの局所に対する治療効果について、PMDAがこれまでの抗がん剤とはまったく異なる見解を示しました。
そもそも、2017年頃に当社が「このような試験を実施したい」とPMDAに話をした際、当社はエンドポイントを生存率に設定していました。通常の抗がん剤でも生存率を重視した設計が一般的です。そのため、当社も同様にPMDAに相談しました。
ところが、PMDAから「あなた方が局所の治療を目指しているなら、局所の効果で承認を取ったらどうですか?」との判断が示されました。これは、当社にとっても願ってもない方向性でした。
この変更によって収益化のプロセスを大幅に短縮することが可能になります。もし仮に生存率をエンドポイントとした場合、1人の患者さまを2年から3年にわたってフォローしなければならず、多くの時間を要することになるためです。
局所の治療については、24週、すなわち半年や1年半といった短期間で決着がつくことになります。PMDAから「短期間で決着をつけるように」と言われて少々驚きましたが、指示に従い進めてきた結果が今日に至ります。
現在は、肛門がんや喉頭がんといった疾患においても、できる限り局所治療で許可を得ることを検討しています。治験期間が最も短い方法で許可を得られるよう、方法を模索しているところです。
吹野執行役員のご説明のとおり、肛門がんは化学放射線療法を行うなどさまざまな治療法がありますが、当社は1点に集中し、局所のがんを消して人工肛門を作らなくてもよくするというエンドポイントを考えています。
この目標を達成するために、人工肛門を作らなくても済むという判断が可能になる新しいプロトコルを構築したいと考えています。
このプロトコルが構築できれば、パイロット試験を経て、本試験を行う予定です。このプロセスにはおおよそ3年から4年が必要と見込んでおり、2030年までには少なくとも効能追加が1つ承認されることを目指しています。
喉頭がんに関しても同様です。声帯を残すことができ、なおかつ再発も防げるような、いわゆる局所で声が出なくなるといったがんの患者さまに対応して効能追加を進めることで、非常にレアなケースでもマーケットを少しずつ拡大していくことを考えています。
2030年までに最低でも1つの適用拡大を目指したいと考えています。株主のみなさまにとっては「少しゆっくりではないか?」と思われる方もいらっしゃるとは思いますが、できるだけ短期間で局所での許可を取得できるよう、PMDAとの話し合いを進めたいと思います。
質疑応答:人種差・個人差の影響について
質問者:アジアを中心に海外展開されるということですが、例えばモンゴル人は中和抗体を持っているというようなことも聞いています。「テロメライシン」の人種差・個人差の影響をおうかがいしたいです。
浦田:「『テロメライシン』には有効性において人種差や個人差があるのか?」について、現時点ではわかりません。
実際に試してみないとわからないところもありますが、有効性に関して中和抗体のお話が出ましたので、1点補足します。
日本人、特にここにいらっしゃる株主のみなさまのうち、おそらく8割から9割の方は子どもの頃に扁桃腺炎にかかった経験があると思います。その場合、「テロメライシン」に対する抗体を持っていると考えるべきです。
それにもかかわらず、今回50パーセントの方に局所で非常に強い効果が見られています。「テロメライシン」は、点滴による投与ではなく、局所に直接ウイルスを注射して感染させる投与方法のため、血液中の中和抗体によって効果が弱まることはないと考えています。
加えて、岡山大学と共同で行った実験では、アメリカ人や日本人などさまざまな人種由来の細胞を使用しました。特に「テロメライシン」の製造時に使用されているがん細胞は、アメリカ人のがん患者のがん細胞を培養して作られています。
このような点から、人種差はそれほど影響しないのではないかと考えています。ただし、実際に治験を行ってみなければはっきりとはわかりません。
一方、個人差に関しては重要な課題と認識しています。今回、50パーセントの方でがんが消失した一方で、残りの50パーセントの方では効果が得られていません。同じ条件で、医師が内視鏡を用いた投与を慎重に行ったにもかかわらず、なぜ半数の方には効果がなかったのかについて、当社としても今後の大きな課題です。
この点については、先生方も強い関心を寄せており、効くケースと効かないケースの関連性を明らかにすることを研究テーマとしたいと考えています。
質疑応答:特許戦略について
質問者:特許戦略について、どのようにお考えか教えていただけますでしょうか?
浦田:「テロメライシン」のもともとの物質特許については、残念ながらすでに切れています。しかし、内視鏡で投与するという2040年までの用途特許は当社が保持しており、少なくとも日本では内視鏡を用いてウイルスを投与することは当社に限られている状況です。
現在、他社でもアデノのオンコリティックウイルスの研究が行われていますが、食道がんを対象とすることはほぼ不可能な状況です。この点は当社の非常に大きな強みであると考えています。今後は、ヨーロッパやアメリカでの特許成立に向けて尽力していく所存です。
質疑応答:「テロメライシン」承認後の収益性について
質問者: 2026年12月期から販売開始すると、製品販売収入だけで黒字化するのでしょうか? 収益性について、どのように考えればよいのでしょうか?
浦田: 「テロメライシン」の薬価や価格は国が決定することになっています。当社としては、有用性加算や先駆け加算などを主張し、できる限り高い薬価を取得したいと考えています。
薬価次第で収益性は大きく変わってきますが、当社としては、今年の夏または秋頃から発売できると想定しています。ただし、発売日からすぐに商品が大きく売れるというわけではありません。病院での審議会や薬価交渉、納入価格など、複雑なプロセスを経る必要があります。今期も売上を見込んでいるものの、発売直後に黒字化することは難しいと考えています。
そのような意味では、2027年から2028年頃にはしっかりとした市場を確立したいと考えています。薬価によっては、その段階で黒字化の可能性も十分にあると見ています。
国内以外に、海外展開についても対応を進めています。当社のビジネス部門で樫原常務を中心に動いており、台湾や韓国をはじめとするアジア諸国での展開を検討しています。特に、内視鏡の普及が進んでいる市場での可能性を追求しています。
タイやシンガポールなどにおいて、日本で正式な許可を取得した薬については、かなり優先的に審査されるのではないかと思います。
なお、条件付き承認や承認間近という段階では、なかなか話を進めるのが難しい状況です。そのため、正式な承認を取得し、信頼できる企業と提携して、市場を拡大していきたいと考えています。
質疑応答:税務上の累損について
質問者:株主総会での減資により、会計上は累損が解消されました。一方で、税務上の累積損失は、まだ大きな数字が残っているのではないかと考えています。どの程度あり、いつから税支払いが開始するのでしょうか?
秦: 先程の浦田社長の説明と重複しますが、薬価が確定し、販売数量が見込め、それが税引き前利益として認識されるタイミングがポイントになります。具体的にいつからになるかは、現時点ではお答えすることが難しい状況です。
また、現時点で税務上の累積損失は、概算で100億円以上あります。但し、税務上の累損は一定期間が経過すると、過去のものから消却されます。期間の定めがない会計上の数値とは異なります。
質疑応答:「OBP-601」の今後のアプローチについて
質問者:「OBP-601」の神経性疾患の一部に、メガ・ファーマが興味を持っているというお話がありましたが、Transposon社を通す以外に現状できることは残念ながらないという理解でいいでしょうか? 「OBP-601」の神経性疾患に関して、現在できるアプローチについてお聞かせください。
浦田:Transposon社にライセンスした「OBP-601」について、当社が何をできるのかについてお答えします。臨床試験は、2025年までの学会発表やデータ解析といった段階で止まっており、なかなか進展が見られませんでした。
しかし、資金獲得に向けてさまざまな努力を行っており、まもなくアメリカ国内で資金調達が行われるという情報を聞いています。
Transposon社との定期会議があるため、その場で進捗状況を確認するだけでなく、早急に臨床試験に着手してもらうための提案や、関係する先生方との具体的な話し合いを働きかけています。
仮に国際治験をやるのであれば、日本を含めてほしいと要望し、日本に進出する際には当社が直接先生方と接触するといった活動を行います。ただし、最終的な判断はすべてTransposon社が行うことになっています。
Transposon社は、「OBP-601」の開発を目的として設立された会社であり、このプロジェクトを軽視しているわけではありません。彼らも必死に資金調達や製薬メーカーとの交渉を進めています。
そのため、もう少し冷静かつ広い視点で捉えていく必要があると考えます。焦りや苛立ちが募る状況ですが、当社も彼らが一刻も早く進めてくれることを望んでいます。また、私自身もTransposon社の社長と定期的に話し合いを重ねています。
日本の株主さまの考え方に加え、当社の意見もしっかりとTransposon社に伝えるよう努めています。このような状況について、何卒ご理解賜りますようお願いします。
質疑応答:高薬価戦略について
質問者:社長が高薬価政策を宣言されているのは、「テロメライシン」に対して自信があるからだと思っています。どのように高薬価を取得するのか教えてください。
浦田: 厚生労働省では、原価が最も重要視され、その上で有用性加算やオーファン加算などのさまざまな加算が付与される仕組みになっています。このため、原価の詳細を調査しなければならないという課題は確かにあります。
一例として、ベルギーのヘノジェン社についてお話しします。ヘノジェン社は、例えば原価や人件費がどれくらいかかったかといった詳細を、当社へ直接開示しません。ただし、ヘノジェン社は、当社を介さずに直接厚生労働省に原価や人件費などの詳細な情報を提出することを約束しています。これにより、当社が詳細を把握しない部分も薬価の原価に反映される仕組みとなっています。
開示率が50パーセント以上になるよう、当社も開示に努めています。ただし、あまりにも高い薬価になると、患者さまが使いにくい薬になる可能性があると私自身も理解しています。
質疑応答:高薬価戦略が海外展開におよぼす影響について
質問者:高薬価戦略が海外展開において、どのような展望をもたらすとお考えでしょうか?
浦田:海外でのライセンス供与やアジアでの販売などについては、あまり高額な薬では広がりが制限される場合があると認識しています。
ただし、みなさまもご存じのように、遺伝子医療で1回3億円以上といった薬価が設定されたり、CAR-T療法として知られる血液がんの治療法では5,000万円や1億円といった高額な薬価が設定される時代になっています。
「テロメライシン」については具体的な薬価はまだ定まっていないものの、これまで当社が投資してきた金額をしかるべき期間内で回収できるような薬価をしっかりと目指していきたいと考えています。
なお、アメリカにおいてはトランプ氏が薬価の引き下げを求めており、今後の動向が不透明である状況です。
質疑応答:富士フイルムとの連携について
質問者:昨年、テレビ東京で「富士フイルムが医薬品の製造ビジネスを行う」と報道していました。これは、御社の「テロメライシン」と関係しているのでしょうか?
浦田:当社の販売については、富士フイルム富山化学という富士フイルムの100パーセント子会社と提携契約を締結しています。富士フイルム富山化学と富士フイルム本体はつながりがあるものの、現時点で当社が話をしているのは富士フイルム富山化学のみです。
テレビでも取り上げられていた製造施設は、富山県にあると思います。2018年から2019年頃に国内外で「テロメライシン」の製造委託施設を探していた際、富士フイルムをはじめとして、ウイルス製造に対して敬遠する企業が多かったという事情があり、国内では施設がなかなか見つからなかった経緯があります。
今後製品が承認され、富士フイルム富山化学に販売をご協力いただき信用が得られれば、さまざまな可能性が考えられると思います。これらを含めて検討を進めていきたいと思います。
質疑応答:「OBP-601(Censavudine)」における抗加齢の発想について
質問者:「OBP-601」の新しい抗加齢に関する質問です。そもそも米国のARPA-Hという組織が、どのように「OBP-601(Censavudine)」に抗加齢に効果があると考えたのか教えていただけますか? また、抗加齢は病気ではありません。治験を行った際に、どのような効能があると判断できるのかについても教えてください。
浦田:まず、「OBP-601」がどのように抗加齢に効くのかについてですが、まだ詳細な情報を確認できていない部分があります。
PSPやALSに関する研究では、脳脊髄液中に含まれるいろいろなバイオマーカーが神経の炎症や老化に関連しており、それが加齢につながるということも指摘されています。ブラウン大学の研究グループが、「OBP-601(Censavudine)」がLINE1を阻害するという発見をしたのも、この文脈の中でのことです。
抗加齢は病気ではなく、むしろ健康な加齢を目指すものです。アルツハイマー病と似た考え方ですが、アルツハイマー病がタウタンパクの蓄積や脳の萎縮といった病理に関連するのに対し、加齢に伴う運動能力や筋力の低下、記憶力の低下といった病気ではない現象に対しての効果の可能性という位置づけです。
あくまで加齢自体は病気ではないため、この研究資金を獲得できたことはうれしく思いますが、治験を含む臨床研究として開始し、脳内物質の変化を観察し、将来的な可能性を検討していく段階にとどまります。そのため、どのような治験を行うのかについては現在のところ明確ではありません。
質疑応答:「OBP-601(Censavudine)」の収益構造について
質問者:アメリカではエイズの治療薬として、すでに「OBP-601(Censavudine)」が販売されているのでしょうか? また、「OBP-601(Censavudine)」はどこで製造しているのでしょうか? Transposon社がどのようになれば、ライセンス収入は発生するのでしょうか?
浦田:「OBP-601(Censavudine)」がHIVに効果があるというエビデンスは示されていますが、エイズ治療薬として認可はされていません。
当社が開発・製造・販売・サブライセンスを含むすべての権利をライセンスしたTransposon社は、抗エイズ薬としての適応ではなく、「脳内のレトロトランスポゾンという浮遊する遺伝子が不適切な箇所に移動しないように抑制する薬」として開発を進めています。南米で治験薬を製造し、カプセル詰めをして治験に使用していますが、まだ治験の段階で販売を開始していません。
Transposon社が資金調達しただけでは、当社にマイルストーン収入は発生しませんが、例えばTransposon社が調達した資金を使って開発を進めて、事前に定めた開発イベントを達成した場合、マイルストーン収入が発生します。また、アルツハイマー病やALS、PSPなどで効果を示した場合、第三者へのサブライセンスの可能性があり、Transposon社が大手製薬会社とライセンス契約を結んだ場合、そのライセンス料の一定額は当社に支払われることになります。
このように、当社が努力して開発したり大手企業を見つけるのではなく、Transposon社の努力で開発が進むことや大手企業とライセンス契約を結ぶことで、当社にも収益が入る仕組みとなっています。
質疑応答:「OBP-702」の治験開始時期について
質問者:「OBP-702」についての質問です。国から3億円の援助を岡山大学が受けて膵臓がんの治験を開始するとうかがっていました。治験の開始時期はいつ頃になりそうでしょうか?
浦田:「OBP-702」については、岡山大学が助成金を獲得し、Phase1を実施できる状況に至っています。これは進行した膵臓がんの患者を対象に、内視鏡を使用して胃まで到達させ、そこから胃内部を通じて膵臓に針を刺し、注入する手法を取ります。
「胃に穴を開けて膵臓がんに注射を行う」と聞くと、この方法に慣れていない方はどのような手順なのか疑問に思われるかもしれませんが、膵臓内にさまざまな物質を注射する際に用いる一般的なアプローチとして、日本国内で実施されています。
Phase1では、この手法を用いて「OBP-702」を低い投与量と高い投与量でスタートします。Phase1が終了した後には、企業治験としてしっかりとした取り組みを進めていきたいと考えています。
すでにPMDAと何度も事前相談を行っており、一部データの不足や臨床に関する文書の改善点について指摘を受けています。ただし、これらの課題も徐々に解決されつつあり、岡山大学が臨床に関連する準備を進めていることから、具体的な進展が見られる予定です。
治験届が提出から30日で特に問題がなければ、年内に第1例目の投与を開始できる見通しです。低い投与量で特に問題がなければ、高い投与量へ移行する予定であり、Phase1の投与は少なくとも来年中には完了すると見込んでいます。
質疑応答:海外での他社の腫瘍溶解ウイルスによる膵臓がんの治験について
質問者:海外の企業によって、アデノウイルスを用いた腫瘍溶解ウイルスで膵臓がんの治験がPhase2まで進んでいるようです。これらは、遺伝子を搭載した次世代腫瘍溶解ウイルスなのでしょうか?
浦田:海外でもいくつか膵臓を対象とした治療が進められているようです。海外のウイルス治療に関しては、遺伝子を挿入した次世代型の腫瘍溶解ウイルスです。
これらのウイルス治療は、さまざまな免疫チェックポイント分子を遺伝子内に組み込んでいるようですが、膵臓への投与が胃の中から行われているのか、点滴や血管からのカテーテルを用いているのかといった詳しい情報はまだ得られていません。
正直なところ、アメリカやヨーロッパでは内視鏡技術があまり得意ではないと認識しています。例えばアメリカでは、内視鏡の施術に全身麻酔が必要で、患者を眠らせて行うのが一般的です。そのため、内視鏡の施術が非常に大変なものになるという特徴があります。その点、日本のほうが実施しやすいのではないかと思います。
膵臓にはがん細胞が効かないいわゆる線維芽細胞が非常に多く存在しており、がん組織に直接注射をするなど、みなさまの想像以上の方法を取らないと効果が出づらい状況です。また、膵臓がんは世界中の大手製薬メーカーが臨床試験に取り組んでいるにもかかわらず、なかなか良い結果を出せない「難攻不落のがん」とされています。
これに対して、あえて「OBP-702」は挑んでいます。治験が十分進んだ段階では「OBP-702」を他のがんにも応用していきたいと考えています。
質疑応答:メルクの今後の展開について
質問者:「テロメライシン」におけるメルクの今後の展開についておうかがいします。胃がんの治験について、具体的にはどのように展開されると想定されていますか?
浦田:メルクとの関係とコーネル大学における治験の進捗についてご説明します。メルクはコーネル大学の治験に対して「ペムブロリズマブ」を無償で提供しており、当社は「テロメライシン」を無償提供しています。このように、コーネル大学が仲介に入るかたちとなっていますが、現時点でメルクから胃がんに対して具体的な意思表示はありません。
現時点で13例中12例を組み入れ、途中経過ではこれまでにレスポンダーが1例出ていると聞いています。ただし、13例すべての組み入れが完了した後に、さらにレスポンダーが何例出るかはわかりません。とはいえ、レスポンダーが1例でも出れば、プラス13例の治験についての判断が可能になるという見解です。
年内に判断があるため、もう少し時間がかかる見込みです。メルクの動向については、臨床試験の結果次第でその可能性がないわけではありません。ただし、特許切れなどのいくつかの問題もあり、今後メルクがどのように対応するかについては、当社としても現時点でははっきりとわかない状況で、予測は難しいです。
質疑応答:Transposon社の資金調達状況について
質問者:Transposon社の資金調達が好転しそうだ、とのお話がありました。その要因について教えていただけますか?
浦田:昨年までは資金調達が進まなかったものの、今年ようやく実現しそうだと聞いています。特別な変化があったというよりも、長期間にわたるネゴシエーションが成果を上げ始めたと考えています。
トランプ政権での政策の変化などが直接的な要因ではないと思いますが、アルツハイマー病創薬財団からの資金提供といったニュースは、投資家にとって非常にポジティブな要素として作用しました。このような動きが、投資へ踏み切るための1つの大きなトリガーになったと考えています。
質疑応答:「テロメライシン」承認に至るまでのリスクについて
質問者: 「テロメライシン」の製造販売承認見通しやそれに伴うリスクについて、社長のお考えを教えていただきたいです。
浦田:「テロメライシン」に関しては、年内半ば頃に承認され、夏から秋頃には発売できると見込んでいます。ただし、これはあくまで当社の見込みです。
リスクについてあえていうと、PMDAの承認における状況や課題に加え、厚生労働省の専門部会において議論される事項が含まれます。専門部会では専門家が集まり、保健医療として本当に必要な製品かが審議されます。
最終的には審査会を通過して正式に承認されることになりますが、現時点でいくつかの審議が残っています。その中でひっくり返される可能性は、限りなくゼロに近いと考えています。
ここまで進んだ段階でひっくり返される可能性は低く、相当ネガティブな情報がない限り、当社の予想どおり進むのではないかと考えています。
当社の薬事担当者からは、PMDAとのやり取りについて逐次報告を受けていますが、大きな方向性が変わるようなドラスティックなリスクはないと思っています。ただし、リスクを最小限にするために、PMDAからの追加質問にもしっかり回答していきたいと考えています。
質疑応答:メディア露出の予定について
質問者:認知度を高めるためや患者さまに希望を与えるために、テレビに出演する予定はありますか?
浦田:テレビ局側から依頼があった場合には喜んで対応したいと考えているものの、現時点で予定はありません。一方で、週刊誌などの取材は受けており、これらを通じてメディアへの露出を増やしていきたいと考えています。
もちろん、今後テレビなどの媒体で取り上げられる機会があれば積極的に参加し、当社のために活用していきたいと思っています。
質疑応答:政府によるバイオ分野戦略としての資金について
質問者:政府がバイオ戦略を推進するために多額の投資を行うようですが、オンコリスが国家から関与を受けている点はありますか?
浦田:政府が推進しているバイオ分野の戦略関連の大規模な資金は、直ちに当社にその恩恵が及ぶ状況にはありません。政府もさまざまな方針を考えており、「iPS」など、特定の分野やプロジェクトに対して資金を振り向けているようです。
その中には抗体の開発に関する取り組みも含まれていると認識しています。いろいろな抗体を作れるようなCDMOと呼ばれる受託製造機関で、製品を作るために資金が使われると聞いています。
当社のように上場しており、まもなく製品が市場に出るような企業には、こうした資金がなかなか回ってきません。ただし、私も機会があればこのような資金も獲得していきたいと考えていますが、お約束できることではありません。まずは、政府の考え方をもう少し詳しく理解していきたいと思っています。
質疑応答:膵臓がん治療における局所治療の考えと将来的な展望について
質問者:「OBP-702」についてです。膵臓がんに対してどの程度の効果が期待できるのでしょうか? 腹腔鏡での投与の可能性はありますか? また、浦田社長は外科のご出身でしょうか?
浦田:まず、私は医師ではなく薬学部出身です。
お話ししたとおり、「OBP-702」については岡山大学第一外科の先生方が実施します。開腹して行う方法では患者さまへの侵襲が非常に大きいため、原則的に開腹を行わない方針です。
また、内視鏡を用いて膵臓に投与する理由についていくつかお伝えします。岡山大学の基礎実験結果から、膵臓がんには、がん細胞ではないものの、がん細胞に栄養を供給したり抗がん剤の浸透を妨げる「がん関連線維芽細胞」という細胞が多数存在します。飲み薬や点滴はもちろん全身に行き渡りますが、こうした細胞の妨害により、抗がん剤が膵臓がん細胞まで十分に届かないというのが岡山大学の認識です。
一方、「OBP-702」は、がん細胞を取り巻くがん関連線維芽細胞に対しても、p53の強力な殺傷効果を有しています。つまり、がん細胞だけでなく、がん組織内に存在する線維芽細胞まで破壊する研究データが得られています。そのため、胃カメラ程度の侵襲で済むような方法、すなわち開腹せずに直接注射する方法が最適との結論に至っています。
ただし、ご指摘のとおり、技術の進歩に伴って腹腔鏡下での施術などが今後取り入れられる可能性は十分にあります。腹腔鏡下で注射が容易な部位のがんであれば、そうした選択肢も考えられるでしょう。この点については、岡山大学第一外科の先生方と情報交換を進めたいと思います。
浦田氏からのご挨拶
長時間にわたり、みなさまからの熱心なご質問にお答えすることができたかと思います。今後も「テロメライシン」承認並びに販売開始後の活動に向けて、全力で取り組んでいきます。引き続きご支援ご指導のほど、よろしくお願いします。本日は長時間ありがとうございました。



