2026年2月18日に開催された、サスメド株式会社2026年6月期第2四半期決算説明会の内容を書き起こしでお伝えします。
ビジョン
上野太郎氏(以下、上野):みなさま、本日はお集まりいただき、誠にありがとうございます。サスメド株式会社 代表取締役社長の上野です。それでは、当社の2026年6月期第2四半期の決算説明を始めます。
まず、当社の紹介です。サスメド株式会社のビジョンは「ICTの活用で『持続可能な医療』を目指す」であり、「SUStainable MEDicine」を略してサスメド株式会社と称しています。
事業領域概要
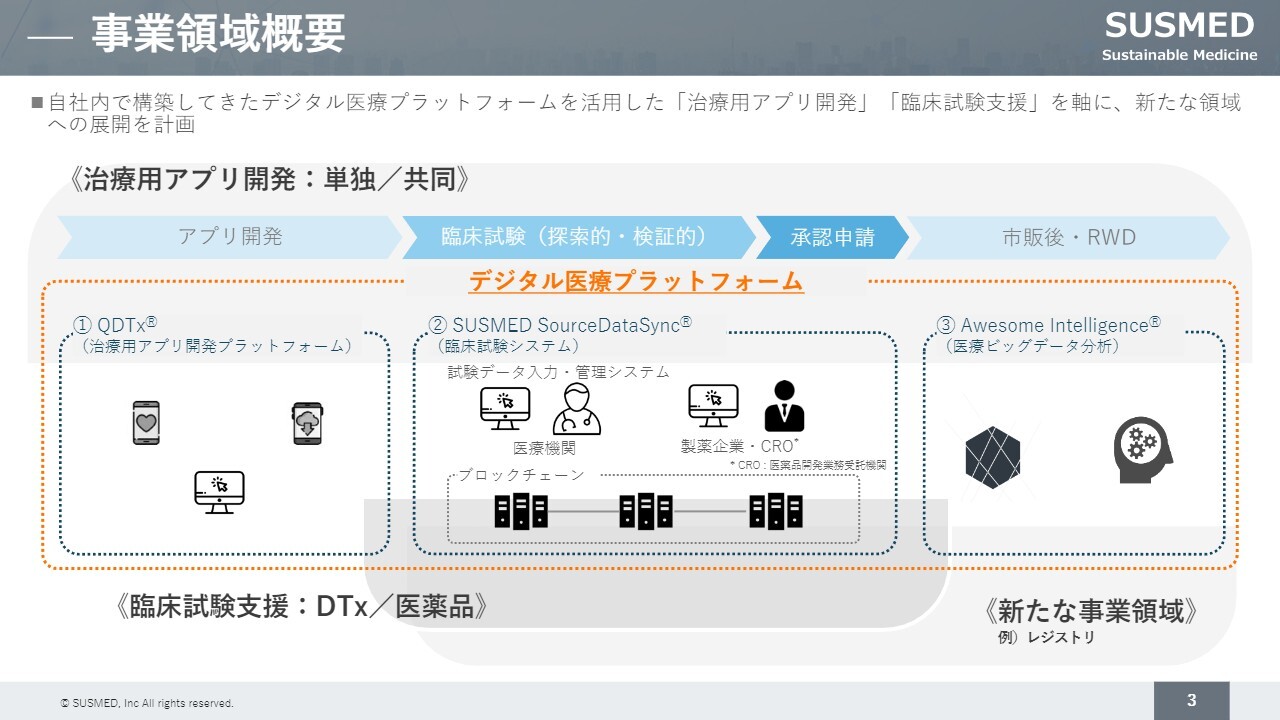
具体的な取り組みについて、まず治療用アプリです。こちらは、疾患を治療するためのアプリを医療機器として承認を受け、上市していく取り組みです。この内容については後ほどご紹介します。
もう1つの大きな取り組みとして、治験のプラットフォームがあります。具体的には、ブロックチェーン技術を活用し、治験で求められる規制対応をシステムで実現する取り組みを行っています。
今後は、上市された治療用アプリを通じて医療ビッグデータを多数扱うことになります。そのため、医療ビッグデータを活用したビジネスも視野に入れています。また、すでにレジストリデータの質をブロックチェーン技術で向上させる取り組みを事業として進めています。
QDTx:治療用アプリ開発プラットフォーム
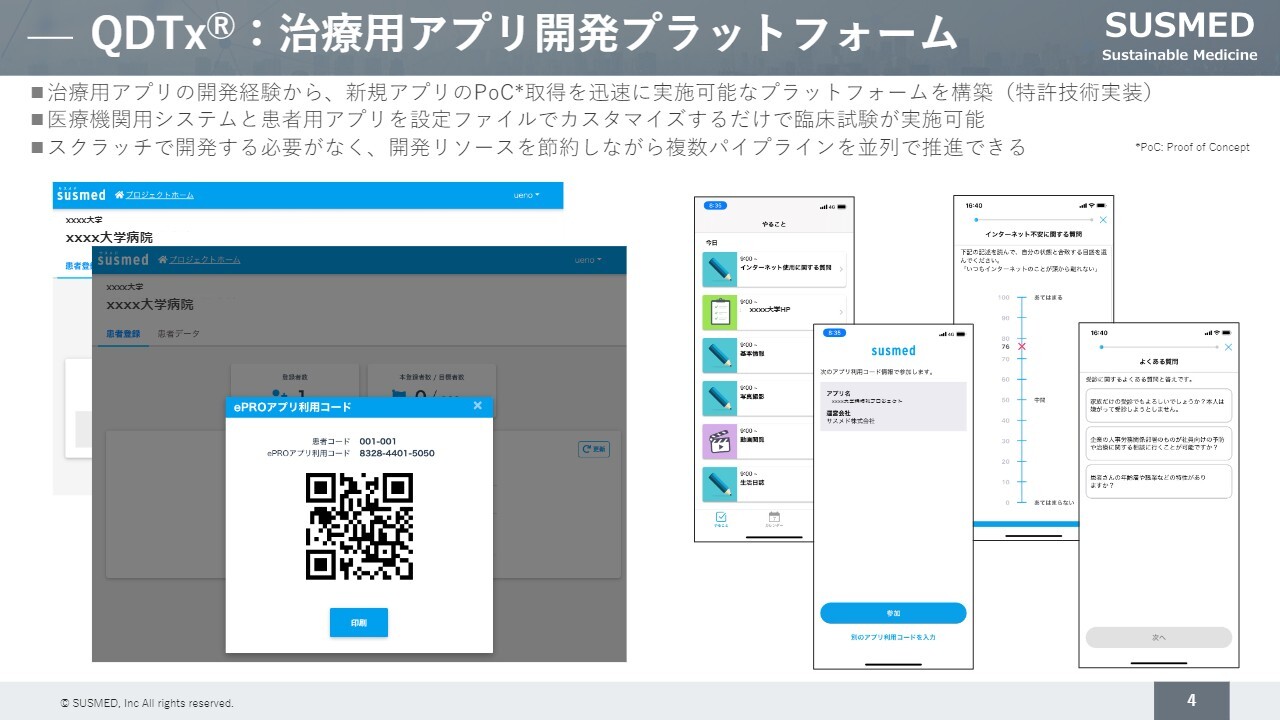
このような取り組みを行う上での当社の強みについてです。現在50名弱のチームですが、それにもかかわらず複数のパイプラインを並列で開発できる点があります。
また、製薬会社の方々とアライアンスを組み、開発段階から共に取り組むことで、当社のケイパビリティに期待いただいている点の1つとして、治療用アプリの開発プラットフォームを有していることが挙げられます。
このような治療用アプリは、アプリを作って終わりではなく、医療機関で治験を実施することが必要です。そのため、仕組みを連動させ、社内の工数を可能な限り節約しながら複数のパイプラインを並列で推進できる基盤となっています。
SUSMED SourceDataSync:臨床試験システム

当社は医療機器メーカーであり、承認を得て製品を上市するためには治験の実施が必要です。製薬メーカーや医療機器メーカーに共通して重要となるのは、臨床試験や研究開発の部分です。
研究開発費の高騰が最近課題となっており、当社は従来の労働集約的な治験業務オペレーションをシステムに代替する取り組みを進めています。
具体的には、ブロックチェーン技術を用いることでデータの信頼性をシステムで担保しています。このシステムは厚生労働省からお墨付きをいただき、GCP省令という規制に準拠したかたちで運用することで、治験の効率化を実現しています。
これにより、当社自身の研究開発費の効率化や資本効率化が可能となり、最近では他社の企業治験などにも導入いただいており、事業の柱となっています。
Awesome Intelligence:機械学習自動分析システム
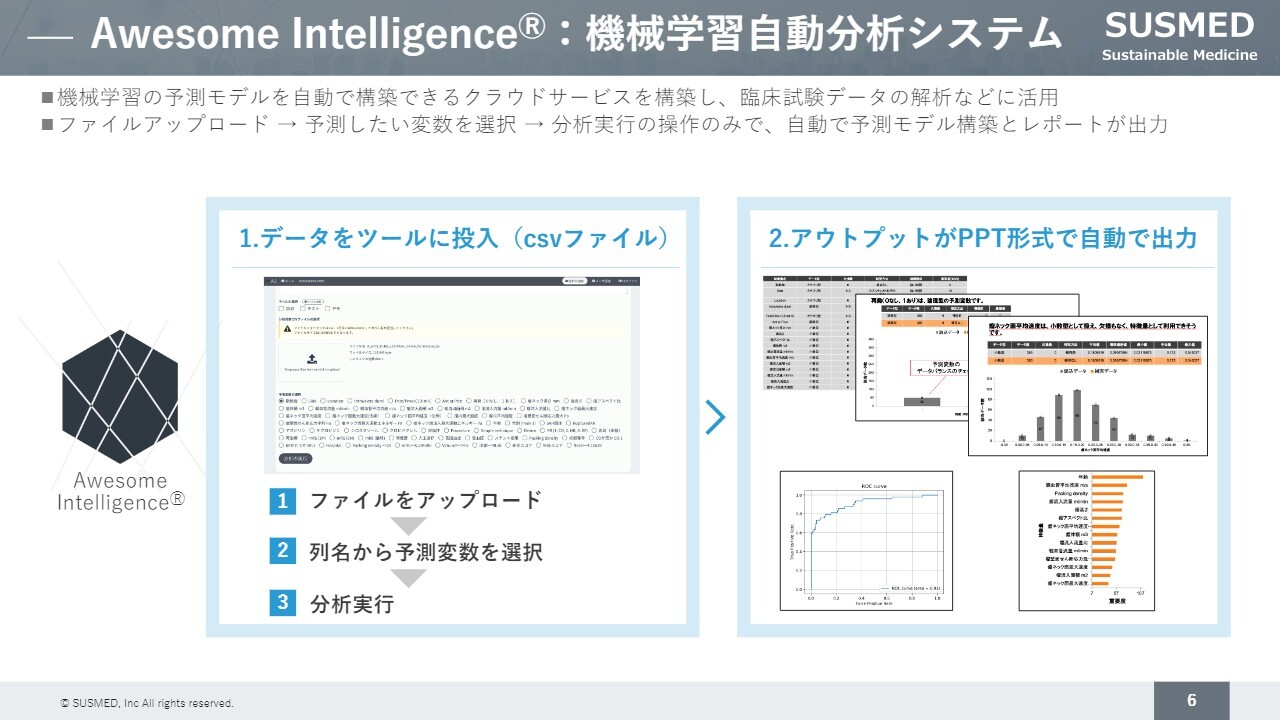
また、今後本格化する予定の部分ですが、医療ビッグデータを機械学習で自動的に分析するシステムやクラウドサービスを構築しています。これを活用することで、将来的には医療ビッグデータを効率的に分析していきます。
現在もアカデミアとの共同研究を行っており、医療ビッグデータの分析や研究開発を進めています。
治療用アプリの提供の流れ
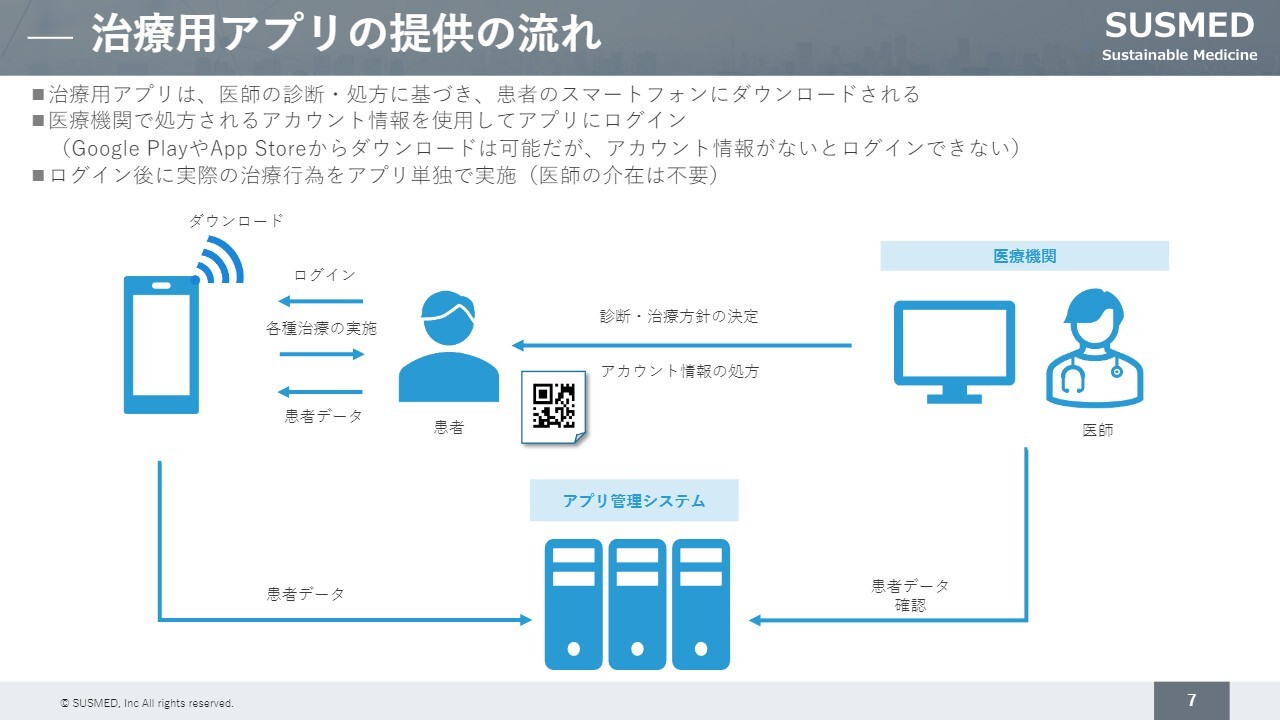
治療用アプリの説明です。これまでにお聞きになった方もいらっしゃるかと思いますが、この治療用アプリは医療機器に該当するため、医師が診断した患者に処方して初めて使用可能なものです。
従来は医薬品の処方箋を発行していましたが、その代わりに治療アプリにログインするためのアカウントを医師が処方し、患者は自身のスマートフォンを使ってそのアカウントでログインし、自宅にいながらこの治療用アプリを通じて治療を受ける仕組みです。
また、日々の治療状況が自動的にアプリ経由でサーバーに送信されます。「薬の飲み忘れ」や「自宅で適切に薬を服用しているか」といった従来は不明だった点が、治療用アプリを通じて明確になります。これにより、患者データを医師が確認し、治療方針の最適化につなげることが可能となります。
ヘルスケアアプリと治療用アプリの違い
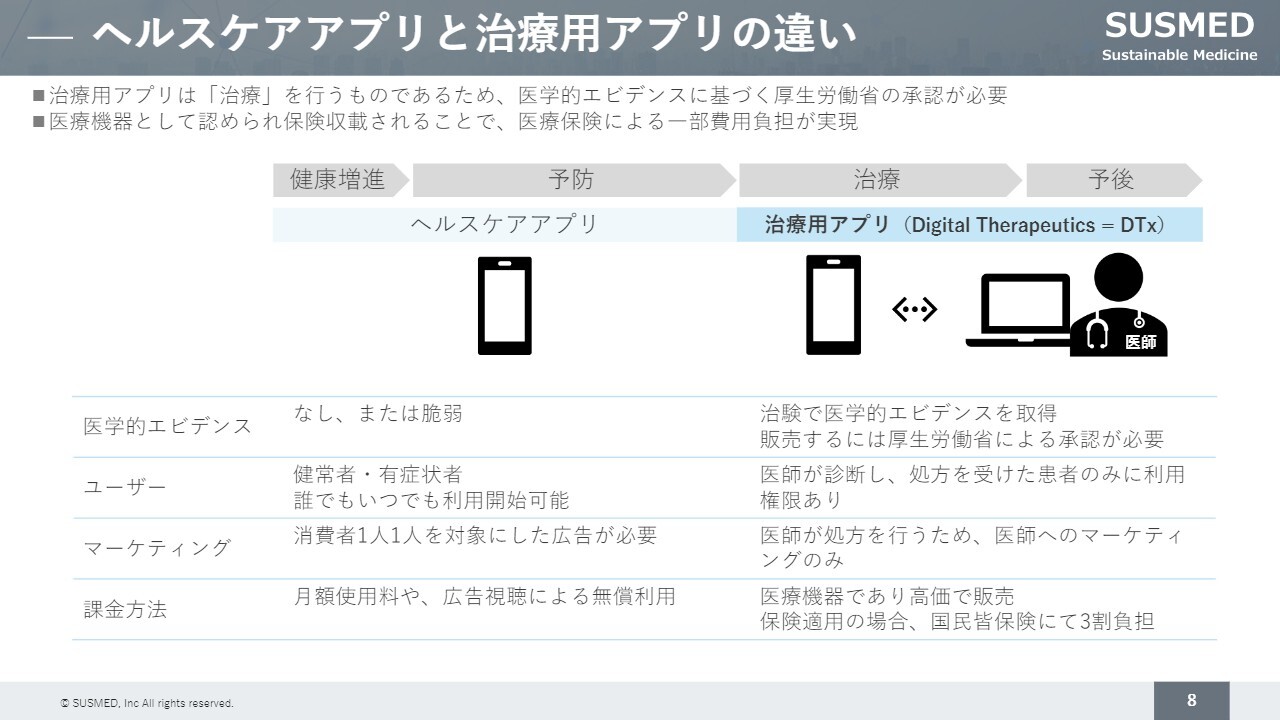
治療用アプリの最大の特徴は、治療を目的としている点にあります。これまで多数存在している健康増進を目的としたヘルスケアアプリとは異なり、治療そのものをアプリを通じて行うことが可能です。
したがって、治験を実施した上で厚生労働省の承認を得て、実際に処方されるものであり、現在その手続きを進めています。また、保険収載されることで、患者の自己負担は3割など一部の負担となる点が特徴です。
開発パイプライン① (2026年2月13日現在)

スライドは当社の開発パイプラインです。不眠障害治療用アプリについては、すでに製造販売承認を取得しており、昨年8月末時点で一部変更申請を行ったものが承認され、9月に保険適用希望書を提出したという状況です。
それ以外にも、後続のパイプラインで現在開発を進めているものとして、がん領域や腎臓病領域、さらに耳鼻科領域における耳鳴りの治療用アプリを杏林製薬と共同で開発しているものがあります。
開発パイプライン② (2026年2月13日現在)
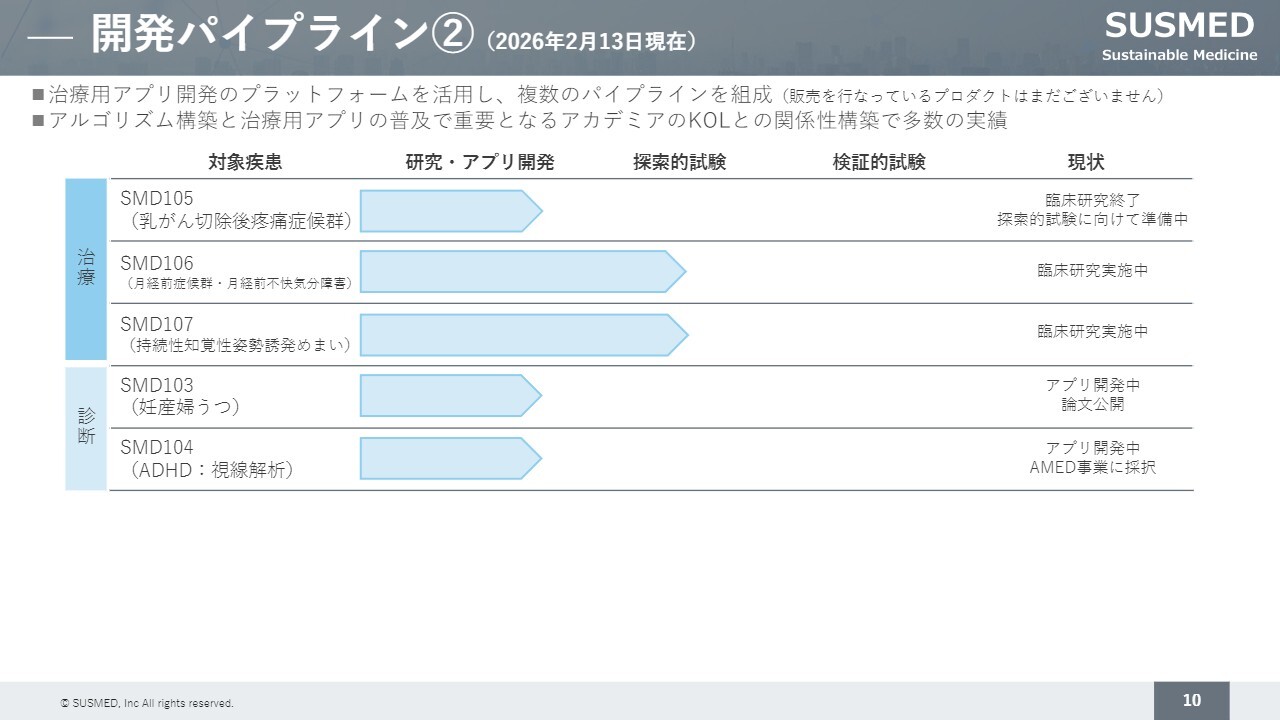
こちらのスライドには、開発中のパイプラインを示しています。例えば、産婦人科領域のPMS(月経前症候群)やPMDD(月経前不快気分障害)に対する治療用アプリを、あすか製薬と共同開発しており、現在特定臨床研究を実施しています。
また、このような治療用アプリに加えて、診断用のプログラム医療機器についても、アカデミアとの共同開発を進めています。
2026年6月期 重点施策
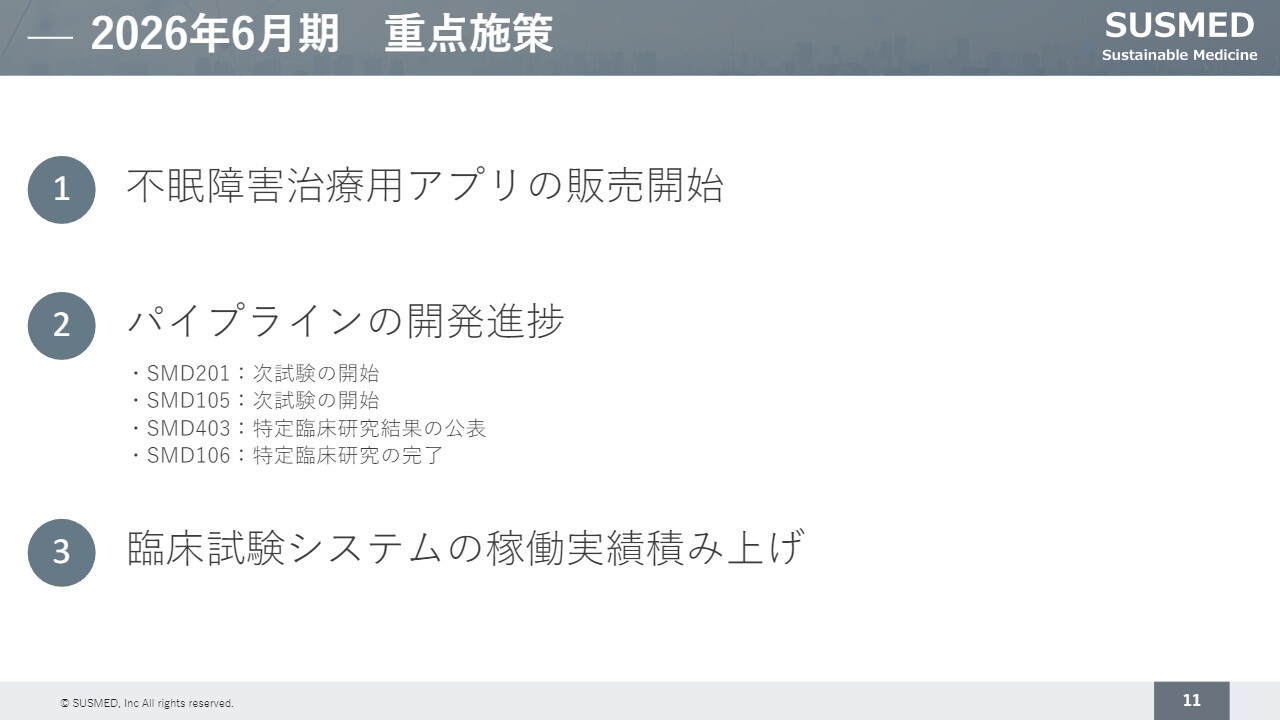
2026年6月期の重点施策をご説明します。当社は3つの重点施策を掲げています。
1点目は、保険収載を経て不眠障害治療用アプリの販売を開始することです。
2点目は、治療用アプリについて、先ほどご紹介した各種パイプラインの開発を進めることです。1点目と2点目は、治療用アプリ事業の重点施策となります。
3点目は、プラットフォーム事業にて、先ほどご紹介したブロックチェーン技術を実装した臨床試験システムの稼働実績をさらに積み上げていくことです。
重点施策①不眠障害治療用アプリの販売開始
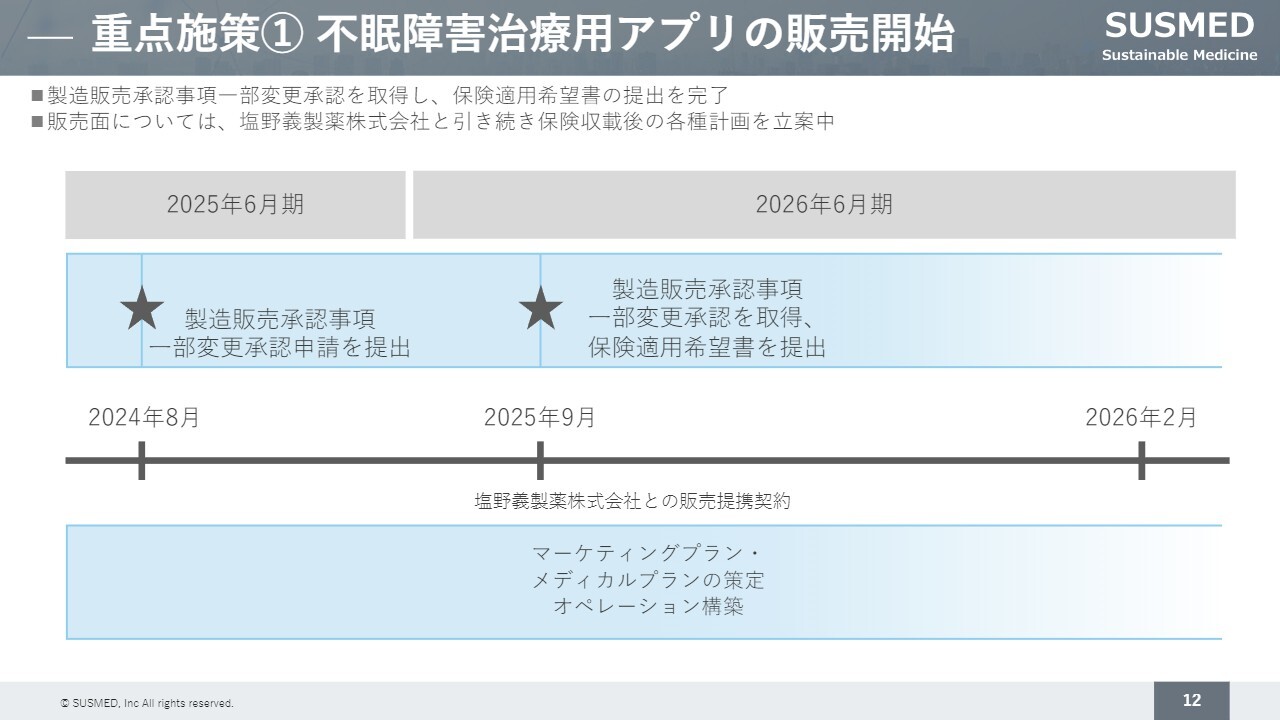
重点施策それぞれの進捗についてご紹介します。不眠障害治療用アプリの販売開始に向けては、2024年8月に製造販売承認事項の一部変更承認申請を提出しました。2025年9月にその承認を取得して、保険適用希望書を提出しています。
当社としては、一日でも早く保険適用され、実際に販売を開始したいと考えていますが、現在は厚生労働省における最終的な中央社会保険医療協議会(以下、中医協)での審議を待っています。
また、不眠障害治療用アプリは、塩野義製薬との販売提携契約が結ばれています。保険適用され次第、上市して全国でご利用いただけるよう準備を進めています。
重点施策②パイプラインの開発進捗 (再掲)

重点施策2点目である後続パイプラインの開発進捗についてです。こちらは前回のIRなどで共有しましたが、杏林製薬との耳鳴治療用アプリが特定臨床研究を実施し、その結果が非常にポジティブだったことを受け、学会発表を行っています。
さらに、杏林製薬との共同研究開発および販売に関する契約について覚書が締結されています。
具体的な内容については開示していませんが、上市を見据え、当社の役割を追加することが合意されました。これに伴い、経済条件としてマイルストーン収入および販売額に応じたロイヤリティが増額されるかたちで、覚書の締結が行われています。
また、杏林製薬のIRなどでも開示されていますが、この耳鳴治療用アプリについては、次の企業治験、いわゆる承認取得のための治験に向けて、できるだけ早く進めるよう、先方とも具体的に進行中です。
重点施策③臨床試験システムの稼働実績積み上げ (再掲)

重点施策3点目のプラットフォーム事業についてです。臨床試験システムの稼働実績の積み上げについては、前回のIRでもご報告しましたが、「iPS細胞から心筋細胞を作り、それを心不全の患者に植え込み治療を行う」という再生医療等製品を開発しているHeartseed社の治験に、当社のブロックチェーンシステムが導入されたという内容がリリースされています。
先方には治験コストの効率化に期待いただき、これまでの当社の実績を評価された結果、実際に導入いただくこととなりました。
iPS細胞等を使用した再生医療等製品での治験導入としてはこれが初めてですが、過去にはアキュリスファーマ社によるフェーズⅢ治験などでも利用されています。このように、さまざまなモダリティ製品の治験へと実績を広げています。
2026年6月期 重点施策の進捗状況
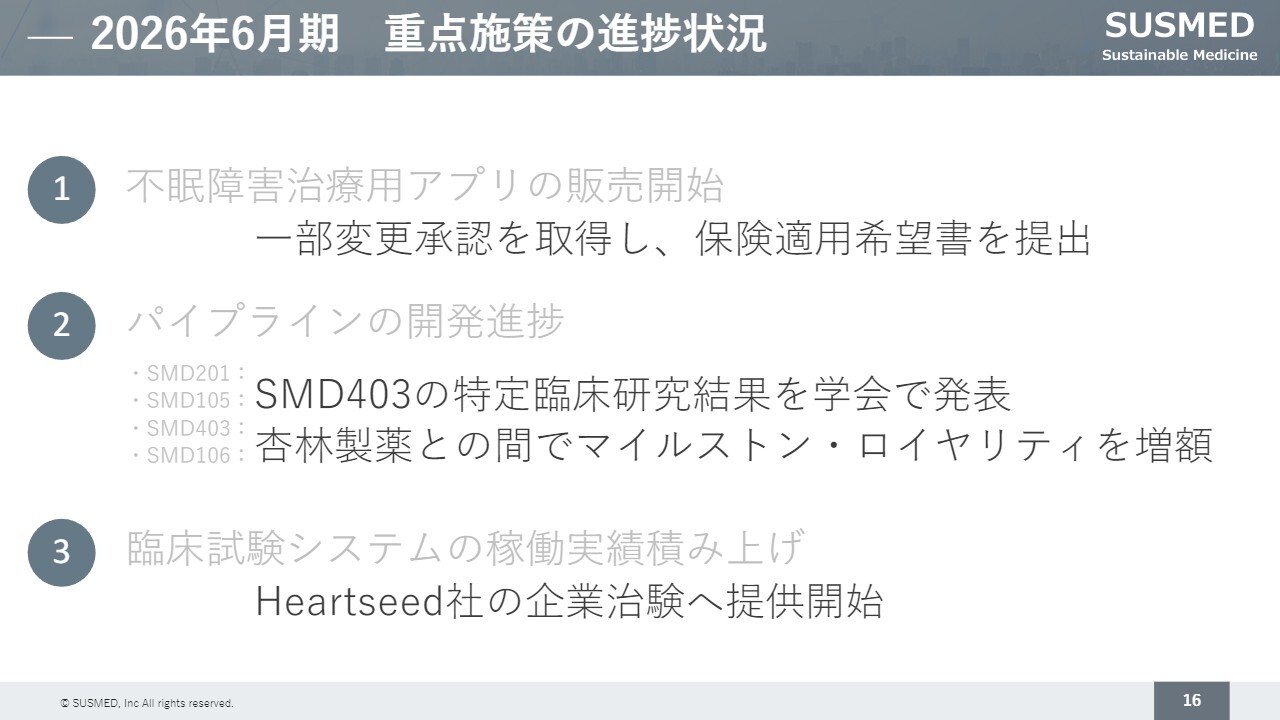
こちらのスライドは、先ほど申し上げた重点施策の進捗状況を示しています。
業績ハイライト
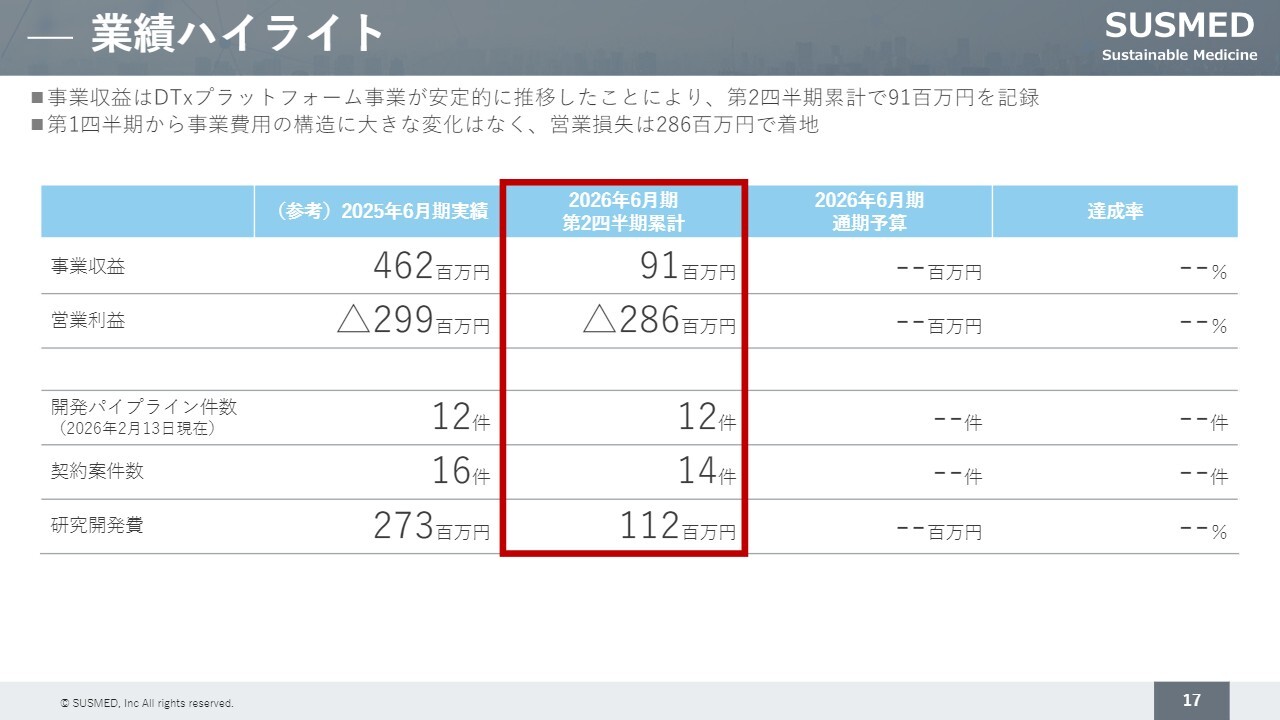
2026年6月期第2四半期時点での業績です。まず、事業収益はDTxプラットフォーム事業での売上が安定的に推移した結果、9,100万円で着地しました。営業利益はマイナス2.8億円です。
セグメント業績
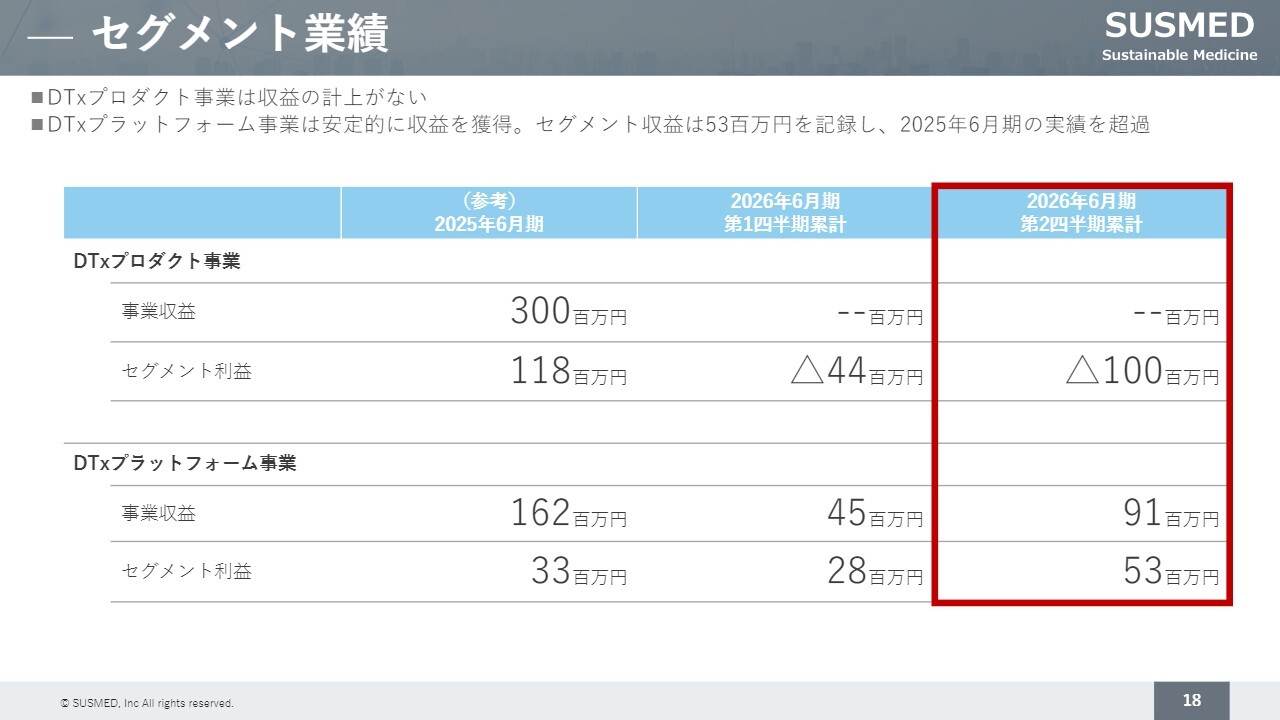
セグメントごとの業績です。今期上半期において、治療用アプリのプロダクト事業に関する事業収益は現時点で計上されていません。参考までに、2025年6月期には3億円のマイルストーン収益がありましたが、今期上半期時点では0円となっています。
売上収益については、先ほど申し上げたDTxプラットフォーム事業での売上収益が上がっています。
財務状況
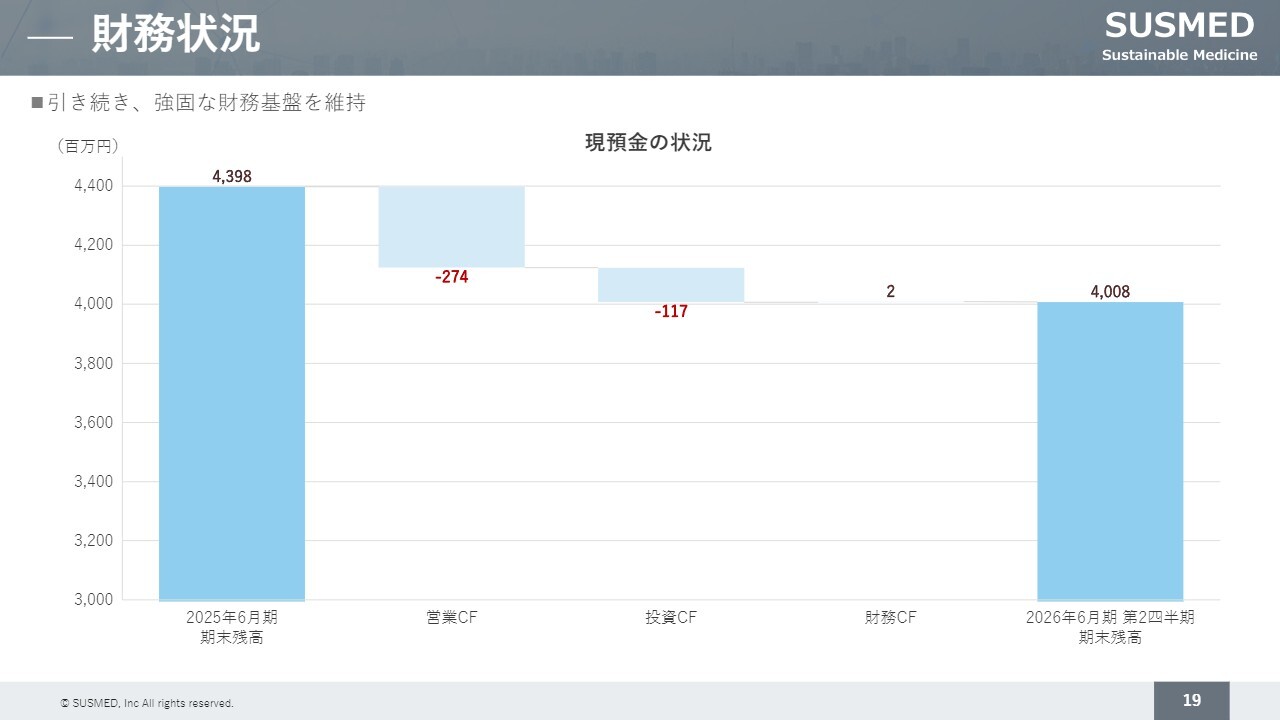
財務状況です。IPO時に資金調達を行い、財務基盤は強固なものとなっています。また、現在も約40億円のキャッシュがあり、安定している状況です。そのため、引き続き研究開発などを進めることができています。
第2四半期のご説明は以上となります。
質疑応答:不眠障害治療用アプリの保険収載のタイミングについて

質問者:不眠障害治療用アプリの保険収載について、そのタイミングや現在の厚生労働省との協議状況をお聞きしたいと思います。具体的にいつ頃を想定しているのでしょうか?
また、業界誌にて、対面による不眠の認知行動療法についても、中医協などで保険収載に向けた議論が進められていると拝見しました。昨年、各学会から「対面治療が保険収載された後にアプリを進める」という手順について声明が出されたとも認識しています。
そのため、順調に進めば、不眠障害治療用アプリにも追い風となるのではないかと推測しています。この点も含めて、現状について共有いただけると幸いです。
上野:公開されている事実に基づいて申し上げます。まず、対面の認知行動療法の不眠症に対する適応の部分です。これは医療機器とは関係なく、いわゆる技術料に該当します。
2年に1回診療報酬改定のタイミングで医療技術評価分科会が開催され、そこで学会から上がってきた要望の技術料について、どれを保険適用の対象として評価するか、評価しないかなどが選定されます。今年の1月中旬、医療技術評価分科会で諮問が出され、その中で対面での認知行動療法が不眠症に対して保険適用されるという方向性が示されました。
技術料と医療機器の特定保険医療材料は独立して評価される前提ではありますが、対面の手法についてすでに保険適用の方向性が示されたことで、アプリについての見通しもご指摘のように明るくなったのではないかと認識しています。
タイミングについてですが、当社は2025年9月に保険適用の希望書を提出しています。これは公開されている情報で、厚生労働省のホームページにも記載がありますが、希望書が提出された翌月から5ヶ月間が保険適用の平均的な審査期間とされています。
そのため、通常であれば10月、11月、12月、1月、2月が審査期間となります。一方で、今年度は診療報酬改定のタイミングが重なっているため、2月中は中医協にて保険適用の審査が行われないと明記されています。
これを考えると、3月以降の中医協で保険適用の審議がなされると認識しています。やり取りの中でなにか問題が発生しているわけではありませんが、診療報酬改定のタイミングもあり、厚生労働省側も多忙な状況にあるのだろうと感じています。これが当社がお伝えできる状況です。
質問者:対面の認知行動療法の保険適用は、6月からでしょうか?
上野:診療報酬改定のタイミングが令和6年度時点で、4月1日ではなく6月1日からとなっていますので、おっしゃるとおりだと思います。
質疑応答:アプリの保険収載について
質問者:アプリの保険収載は対面と同じタイミングか、それとも少し後くらいをメインのストーリーとして考えたほうがいいのか、なにか共有できる点やヒントがあればお願いします。
上野:おっしゃるように、同じタイミングになる可能性があります。医療機器の保険適用のタイミングは3月、6月、9月、12月となっており、3月以降の中医協で保険適用の審議がなされると考えると6月1日からの保険適用が想定されます。
先ほどお伝えしたとおり、診療報酬改定のタイミングでは2月に中医協が開催されないルールがあるため、最短のターゲットは6月1日のタイミングになるのではと考えています。また、それより遅れることは現時点では想定していません。
質疑応答:中医協が開かれるタイミングについて
質問者:6月1日から保険収載となる場合、中医協が開かれるタイミングは3月か4月頃と見ておけばよいでしょうか? また、この議論の情報が対外的に公表されるかどうかについても教えていただけますでしょうか?
上野:医療機器の保険収載に関する中医協の開催については、公表されるかと思います。少なくとも前例では中医協の議題として上がっており、そこで対外的に公表されるタイミングが訪れるのではないかと考えています。
質問者:その中医協の時期は3月や4月頃と考えていてよいのでしょうか?
上野:当社でタイミングを正確に把握することはできません。ただし、仮に6月1日に保険収載される場合、それ以前の中医協で承認される必要があります。そのため、3月、4月、場合によっては5月に承認される可能性があると考えています。
質疑応答:治療用アプリの上市後の売上イメージについて
質問者:6月1日以降の売上について、市場導入も近づいてきた中で、上野氏が思い描いているイメージをあらためて共有していただけますでしょうか? 他社のアプリでは減酒や高血圧に関連したものがすでに上市されているものの、もちろん定量的な開示はありませんが、あまり売上が良くないとの評判が聞こえてくるようです。
以前から「これは少し質の違うものである」というご説明をされており、それについては重々承知しています。ただし、上市が近づくタイミングで、さまざまな学会等で上野氏がお話しされている中で、6月1日に保険収載されてまずどのように使用されるのか、その後の立ち上がりのイメージ等について、もしアップデート可能な情報があればご共有いただけますか?
上野:ご指摘のとおり、学会やセミナー等でお話しする機会を多くいただいています。先日も精神科系の学会の教育セミナーで発表をご依頼いただき、お話をしました。また、今後開催される学会等でも発表の機会が予定されている状況です。
おっしゃるように、治療用アプリをひとまとめにできるものではないという点は、これまで一貫して申し上げているところです。やはり、製品のポジショニングや他の治療法との関係性、その治療法がその分野で実際に求められているのかといった点が非常に重要な要素であると考えています。
不眠症の分野においては、睡眠薬の適正使用が強く求められている状況があります。また、先ほどの議論にもあったとおり、認知行動療法が保険適用となる背景には、非薬物療法である認知行動療法を推奨する流れがあります。
これも以前から申し上げているように、海外のガイドラインでは薬物療法ではなく認知行動療法を第一選択肢として明記している点が強調されています。
さらに踏み込むと、治療用アプリによる認知行動療法が薬よりも優先されることが明記されています。当社の製品はそのようなポジショニングを狙っています。
実際に医師の方からの関心も非常に高い領域であり、学会でご招待をいただいているのも、その表れであると認識しています。
質疑応答:プラットフォーム事業の競合環境と優位性について
質問者:プラットフォーム事業のアップデートについておうかがいします。外部から見ると、競合や参入メーカーが徐々に増加しているように見受けられますが、競合環境や治験サポート関連の競合状況がどのように変化しているか、またその中で御社の優位性、特にブロックチェーンを活用した取り組みが引き続き評価されているかについて教えてください。
上野:おっしゃるとおり、治験分野で効率化を目指すサービスを提供する会社が増えていると認識しています。例えば、遠隔診療のプラットフォームを治験に活用する取り組みを行うベンチャー企業なども出てきています。
一方で、当社はブロックチェーン技術を臨床試験に応用するという特許技術を保有しています。この技術については政府から通知が出されており、治験時にデータの信頼性を担保する必要があるGCP省令に関するレギュレーションを、当社のブロックチェーン技術を用いて代替することが可能だとされています。この点において、当社は独自の優位性を持つプレイヤーだと認識しています。
次に、治験のCRO企業の売上に占める割合についてです。当社の業務は、モニタリング業務をブロックチェーン技術で代替するものですが、CRO業務の売上の半分ほどがモニタリング業務に割かれていることが公開されています。そのため、非常にインパクトの大きい部分をブロックチェーン技術で代替しています。
一方で、先ほど申し上げた遠隔診療のプラットフォームを治験に活用する事例については、あくまで患者が病院を受診する必要がなくなるというメリットを持つにとどまるのではないかと考えます。そのため、CROの売上の半分に匹敵するほどのインパクトがあるとは、当社としては認識していません。
さまざまなプレイヤーが増加しているのはこの領域での課題感の大きさの現れと理解していて、その中でも当社が担っている領域は非常にインパクトが大きく、さらに特許権含む知的財産権で保護された参入障壁のある事業領域であると認識しています。
質疑応答:アキュリスファーマ社の企業治験データについて
質問者:プラットフォーム事業が加速度的に進展するためには、アキュリスファーマの企業治験の進捗が必須であり、その点が重要なポイントであるように思われます。以前から議論に挙がっていると思いますが、あらためて状況を整理して共有いただけますでしょうか?
上野:ご指摘のとおり、横展開を進める上で重要なのは、アキュリスファーマのような事例で医薬品が実際に承認されることです。それが当社にとっても重要なステップであると認識しています。
その実績により、バイオベンチャーだけでなく、中堅・大手以上の製薬企業での活用場面も広がっていくのではないかと考えています。現在は主にバイオベンチャーで実績を積んでいますが、中堅・大手の製薬企業へも展開していきたいと考えています。
質問者:アキュリスファーマの件について、申請や承認の時間軸でコメントできることはありますか?
上野:その点についてはアキュリスファーマの裁量の範囲かと思いますが、アキュリスファーマを買収したViatrisのグローバルリリースでは、すでに承認申請を行ったとされています。
日本では承認申請から1年程度で承認に至るケースが一般的かと思われますので、それくらいの時間軸になると思います。そこで次のステップが生まれるのではないかと期待しています。